바이오연료 지질 및 카로티노이드 색소 생산을 위한 국내 내열성 미세조류 스크리닝
 ; Hyoji Yu2)
; Hyoji Yu2) ; Jeong Hyeon Kim3)
; Jeong Hyeon Kim3) ; Minsuk Park4)
; Minsuk Park4) ; Hyung-Sool Lee5)
; Hyung-Sool Lee5) ; You-Kwan Oh6), *
; You-Kwan Oh6), * ; Soo Youn Lee7), *
; Soo Youn Lee7), *
© 2025 by the New & Renewable Energy
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Thermotolerant microalgal strains have significant potential for industrial applications under heat-stress conditions. In this study, microalgal samples were collected from Gwangju Stream, Korea, and cultured photosynthetically at 40°C to screen for high growth and lipid productivity. Among the 12 candidates identified, Chlorella sp. KR-11 (GJ-1) exhibited the highest biomass production (1.08 g/L) and lipid content (25.7 g/100 g cell). Although biomass, lipid, and carotenoid contents were marginally reduced at 40°C compared to those at 30°C, notable metabolic adaptations were observed. Heat-stress induces a shift in fatty acid composition, which is characterized by an increase in saturated fatty acids and a decrease in unsaturated fatty acids. Similarly, carotenoid synthesis was altered, with reduced lutein and neoxanthin levels but increased β-carotene and zeaxanthin concentrations. These findings demonstrate the metabolic flexibility and thermotolerance of GJ-1 and highlight its potential for biofuel production and high-value pigment synthesis at elevated temperatures.
Keywords:
Microalgae, Thermotolerance, Lipid production, Biofuel, Carotenoid pigment키워드:
미세조류, 내열성, 지질생산, 바이오연료, 카로티노이드 색소1. 서 론
미세조류는 광합성을 통해 이산화탄소를 고정하여 지질, 단백질, 탄수화물, 색소 등 다양한 유기물을 생산하는 미생물로, 재생 가능성과 환경 친화성을 바탕으로 바이오연료, 바이오플라스틱, 식품, 사료, 화장품, 제약 등 다양한 산업 분야에서 주목받고 있다.[1~4] 특히 미세조류가 생산하는 지질은 기존 석유 기반 연료 및 화학물질을 대체할 수 있는 유망한 대안으로 평가된다.[1]
전 세계적으로 약 20만에서 수백만 종의 미세조류가 존재하는 것으로 추정된다.[4,5] 그러나 현재 산업적으로는 활용되고 있는 종은 클로렐라(Chlorella), 해마토코쿠스 (Haematococcus) 등 약 15종에 불과하며, 주로 식품 및 사료 생산에 제한적으로 이용되고 있다. 미세조류의 성장과 생산성은 빛, 영양소, 온도 등 다양한 환경적 요인에 크게 좌우되며, 대규모 생산을 위해서는 경제적이고 효율적인 배양 조건과 균주의 선택이 중요하다.[5]
미세조류는 5°C에서 40°C까지 다양한 온도 범위에서 성장할 수 있지만, 대부분의 균주는 최적 성장 온도가 20°C에서 30°C 사이로 알려져 있다.[5,6] 그러나 미세조류의 산업적 활용을 위한 옥외 배양 환경에서 여름철의 경우 온도가 40°C를 초과하거나, 최대 55°C에 이를 수 있어, 이는 미세조류 성장에 부정적인 영향을 미친다.[2,7] 고온 환경에서는 광합성 효소의 비활성화와 분해로 인해 세포 성장이 억제되거나 사멸하여 생산성이 급격히 감소한다.[5,8~10] 이러한 문제를 해결하기 위해 배양 시스템의 온도를 30°C 이하로 유지하는 방법이 이상적이지만, 초기 투자와 운영 비용이 높아 경제적 실현 가능성은 낮다.
이를 극복하기 위해 여름철 고온 환경에서도 생장과 생산성을 유지할 수 있는 내열성 미세조류 균주의 개발이 필수적이다. 내열성 균주는 고온 환경에서도 안정적이고 경제적인 대규모 배양을 가능하게 하여 바이오연료 및 다른 유용물질의 생산성을 향상시킬 잠재력을 지닌다.[5,10~12]
최근에는 무작위 돌연변이 유도(Random Mutagenesis)와 실험실 적응 진화(Adaptive Laboratory Evolution, ALE) 기술을 활용하여 내열성 및 다양한 환경 스트레스에 강한 균주를 개발하려는 연구가 활발히 진행되고 있다.[11~13] 무작위 돌연변이 유도 기술은 자외선, 이온 빔, 상온 플라즈마 등 물리적 방법과 EMS(Ethyl Methane Sulfonate)와 같은 화학적 방법을 통해 미세조류의 유전적 다양성을 증대시킬 수 있다. 특히, EMS는 DNA의 C/G에서 A/T로의 전이를 유도하여 내열성 돌연변이를 효과적으로 생성하는 화학적 유도제로 주목받고 있다. 실험실 적응 진화(ALE)는 시간이 지남에 따라 환경 스트레스를 점진적으로 증가시키는 방식으로 미세조류가 환경 변화에 적응하도록 유도하는 기술이다. 이러한 기술들을 접목하면 내열성과 함께 다양한 환경 스트레스에 강한 고성능 균주를 개발할 수 있으며, 이는 바이오연료 생산 등 산업적 활용에 크게 기여할 것으로 기대된다.[12]
본 연구에서는 옥외 대량 배양 환경에서 여름철 고온 조건(모델 온도: 40°C)에서도 우수한 생장과 지질 생산성을 보이는 미세조류 균주를 선별하고자 하였다. 이를 위해 광주천에서 다양한 미세조류 샘플을 채집하여 생장과 지질 생산이 뛰어난 균주를 선별하였다. 선별된 균주의 우수성을 기존 모델 균주와 비교하여 검증하고 생물학적 동정을 수행하였다. 또한, 균주의 생장 패턴과 지질 및 카로티노이드 함량을 분석하여 균주의 특성을 규명하였다.
2. 실험 재료 및 방법
2.1 미세조류 분리 및 내열성 선별
호남 지역 광주천 인근에서 담수 샘플을 채취한 뒤 냉장상태로 보관하였다. 채취한 50 mL 샘플은 200 mesh(75 µm) 망을 이용해 여과한 후, 4,000 rpm에서 10분간 원심분리(Centrifuge 5804R, Eppendorf, USA)하여 상등액을 제거하고 최종 부피를 1 mL로 농축(50배)하였다. 배양에는 BG-11(Table 1 참조)를 사용하였으며, 탄소원은 교반을 통해 공기 중의 이산화탄소를 제공하였다. 농축 샘플 1 mL를 100 mL의 배지에 접종하여 250 mL 삼각 플라스크에 담고, 30°C Shaking Incubator(ISS-3075R, JEIO Tech, Korea)에서 150 rpm 조건으로 3주간 배양하였다.
배양된 샘플은 15 g/L Agarose와 50 µg/mL Ampicillin을 포함한 N8 배지(Table 2 참조)에 10 µL씩 도말한 후, 40°C Growth Chamber에서 2주간 배양하였다. 이 과정에서 형성된 콜로니 중 20개를 선별하여 각각 5 mL N8 배지가 담긴 시험관에 접종한 뒤, 40°C Shaking Incubator에서 150 rpm으로 2주간 배양하고 순수 분리 후 계대배양을 실시하였다.
내열성이 우수한 미세조류를 선별하기 위해 순수 분리된 미세조류를 N8 배지 100 mL가 담긴 250 mL 삼각 플라스크에 OD660nm 값이 0.2가 되도록 접종하였다. 이를 40°C, 150 rpm 조건의 Shaking Incubator에서 2주간 배양하였으며, 광량은 LED 조명을 통해 100 µmol photon/m2/s로 유지하였다.
2.2 생물학적 분류 동정
최종 선별된 순수 미세조류의 분자생물학적 종 동정을 위해 N8 고체 배지에서 콜로니를 형성한 후, 순수 콜로니로부터 26S rRNA와 ITS(Internal Transcribed Spacer) 유전자 서열을 증폭하였다. 26S rRNA 유전자 증폭에는 프라이머 LR0R(5'-ACC CGC TGA ACT TAA GC-3')과 LR7 (5'-TAC TAC CAC CAA GAT CT-3')을, ITS 증폭에는 ITS5(5'-TCC GTA GGT GAA CCT GCG G-3')와 ITS4 (5'-TCC TCC GCT TAT TGA TAT GC-3')를 사용하여 PCR을 수행하였다. 이후 확보한 염기서열은 NCBI의 BLAST를 통해 데이터베이스와 비교 분석하였다. 염기서열 분석 결과는 MEGA 11 프로그램(https://www.megasoftware.net/)을 이용해 계통도 분석에 활용되었다.
2.3 온도별 미세조류 배양
최종 선별된 미세조류의 내열성을 평가하기 위해 30°C와 40°C 두 가지 온도 조건에서 배양을 진행하였다. 500 mL 삼각 플라스크에 200 mL N8 배지를 사용하고, 초기 OD660nm 값을 0.2로 맞추어 접종하였다. 광합성 배양은 LED 조명이 장착된 Shaking Incubator에서 100 µmol photon/m2/s의 광량과 150 rpm 조건으로 2주간 진행되었다.
2.4 분석 방법
40°C에서 2주간 배양한 각 미세조류 샘플 20 μL를 Particle Sizer and Counter(Multisizer 4e, Beckman Coulter, Inc., USA)를 사용해 단위 부피당 세포의 개수와 크기를 측정하였다.
미세조류의 형태는 Zeiss Axiolab 광학현미경(Carl Zeiss, Germany)을 사용해 400배율로 관찰하였고, Zeiss Axiocam 506 color 카메라로 촬영하였다.
미세조류 배양액 5 mL를 진공 여과 장치(Nalgene™ Polysulfone Reusable Bottle Top Filter, Thermo Fisher Scienetific, USA)를 사용해 GF/C 여과지(47 mm, Whatman, United Kingdom)에 여과한 뒤, 60°C 오븐(JSON-150, JS Research Inc., Korea)에서 하룻밤 동안 건조하였다. 여과 전후 필터의 무게를 측정하여 건조중량을 계산하였다.
미세조류의 성장은 UV-Vis Spectrophotometer(Bio-Spectrometer® kinetic, Eppendorf, Germany)를 660 nm에서 흡광도를 측정하여 평가하고, 이를 바탕으로 성장 곡선을 도출하였다.
동결건조된 미세조류(10 mg)를 Chloroform: Methanol (2:1, v/v) 혼합용매 6 mL로 초음파 처리(Daihan Scientific, Korea)하여 1시간 동안 지질을 추출하였다. 추출물에 물(1 mL)을 첨가해 Vortexer(Vortex 3, IKA, Germany)로 10분간 혼합한 후, 4,000 rpm에서 10분간 원심분리하여 물층과 용매층을 분리하였다. 용매층(Chloroform)을 주사기로 추출한 후, 0.2 μm의 PTFE 필터로 여과하여 무게가 측정된 유리 바이알에 담았다. Chloroform을 후드에서 자연 증발시킨 후 바이알의 무게를 측정하여 지질함량을 계산하였다.
지방산 메틸 에스터(Fatty Acid Methyl Ester, FAME) 분석은 Bligh and Dyer 방법을 변형해 수행하였다.[14] 동결건조된 미세조류(10 mg)를 Chloroform:Methanol (2:1, v/v) 혼합용매에 담아 지질을 추출한 후, Methanol(1 mL)과 황산(375 μL)을 첨가하여 100°C Heating Block (Thermo Bath ALB64, FINE PCR, Korea)에서 10분간 에스터 교환 반응을 수행하였다. 반응 후 냉각된 샘플에 뒤 증류수(1 mL)를 첨가하고, 5분간 혼합한 다음, 4,000 rpm에서 10분간 원심분리하여 용매층을 분리하였다. 분리된 용매층은 0.2 μm PTFE 필터로 여과하여 HP-INNOWAX(30 m × 0.32 mm × 0.5 µm, Agilent Tech., USA) 컬럼과 Flame Ionization Detector(FID)가 장착된 가스크로마토그래피(Agilent Tech., USA)로 분석하였다.
동결건조된 미세조류(2 mg)는 마이크로 비드(1.0 g)와 Dichloromethane:Methanol(1:1, v/v, 0.025 M NaOH 포함) 용매(1 mL)이 포함된 2 mL 튜브에 넣고, Prep-24 Bead-Beater(MP Biomedicals, USA)를 사용해 6 m/s의 속도로 30초씩 3회 파쇄하였다. 추출물은 비누화 과정을 거쳐 0.2 μm PTFE 필터로 여과하였다. 이후, YMC Carotenoid Column(C30, 5 µm, 250 × 4.6 mm, YMC Co., Ltd., Japan)과 Diode Array Detector(DAD)가 장착된 HPLC (High Performance Lipuid Chromatography, Agilent Tech., USA)로 분석하였다.[15]
3. 결과 및 고찰
3.1 미세조류 순수 분리 및 형태학적 특성 파악
광주천에서 순수 분리한 미세조류 중, 40°C에서 성장이 확인된 12개 후보군을 확보하였다. 형태적으로 이들 미세조류는 크게 두 가지 군집으로 구분되었다. 구형 단일 세포 군집과 초승달 형태로 여러 세포가 연결된 군집이었다(Fig. 1 참조).

Morphology of microalgae isolated from southern Korea observed under an optical microscope (Green text: Circle shape, Gray text: Lunate shape)
이들 후보군은 40°C에서 2주간 배양한 후 1차 선별되었다. 세포 농도와 평균 크기를 비교한 결과는 Fig. 2에 나타내었으며, 비교 대상으로 Chlorella sp. KR-1(KCTC0426BP)과 M082(KCTC11998BP)를 포함하였다. 이들 대조군은 산업 부생가스와 같은 고온의 이산화탄소 배양 조건(35°C 이상)에서 우수한 바이오매스 생산(1.0~1.4 g/cell/L/day) 균주로 국내 특허에 등록되었다.[16,17]

Growth and average cell size of microalgae isolated from southern Korea under photosynthetic flask culture condition at 40°C. Chlorella sp. KR-1 and M082 were compared as model strains for industrial flue gas applications. The results are reported as the mean ± S.D. (n=3)
세포 개수 및 크기 측정 결과 크게 세 가지 그룹으로 분류되었다. 구형 세포 군집 중 GJ-1과 GJ-2는 단위 부피당 세포 농도가 각각 74.41×106/mL와 50.71×106/mL로 다른 후보군 및 대조군보다 높았으며, 평균 세포 크기는 각각 3.325 μm와 3.352 μm로 작게 나타났다. 반면, GJ-5, GJ-15, GJ-19 군집은 단위 부피당 세포 농도가 각각 9.44×106/mL, 7.90×106/mL, 13.59×106/mL로, 평균 세포 크기는 4.346 μm, 4.227 μm, 4.433 μm로 측정되었으며, 대조군인 Chlorella sp. KR-1 및 M082와 유사한 경향을 나타내었다.
초승달 형태 군집은 Fig. 2에서 짙은 회색 막대로 표시되었으며, 단위 부피당 평균 세포수는 14.87×106/mL, 평균 세포 크기는 6.536 μm로 나타났다. 현미경 관찰 결과, 대부분의 세포가 4개씩 연결된 초승달 모양을 형성했으며, 형태학적으로 유사한 특징을 보여 Scenedesmus sp.로 추정되었다(Fig. 1 참조).[18]
3.2 미세조류 건조중량 및 지질 함량 확인
구형 미세조류 후보군 중 높은 세포 농도 또는 상대적으로 큰 세포 크기를 가진 GJ-1, GJ-5, GJ-19를 선택하였으며, 유사한 세포크기를 보유한 후보군(GJ-2, GJ-15)의 경우 세포 개체수가 많은 후보군을 선정하였다. 선정한 후보군(GJ-1, GJ-5, GJ19)은 담수 샘플로부터 고온 성장 미세조류 선별하기 위해 배양했던 온도 조건인 40°C에서 2주간 배양한 후 각 균주의 건조중량과 지질함량을 분석하였다(Fig. 3 참조). 대조군으로 Chlorella sp. KR-1 및 M082를 사용하였다.
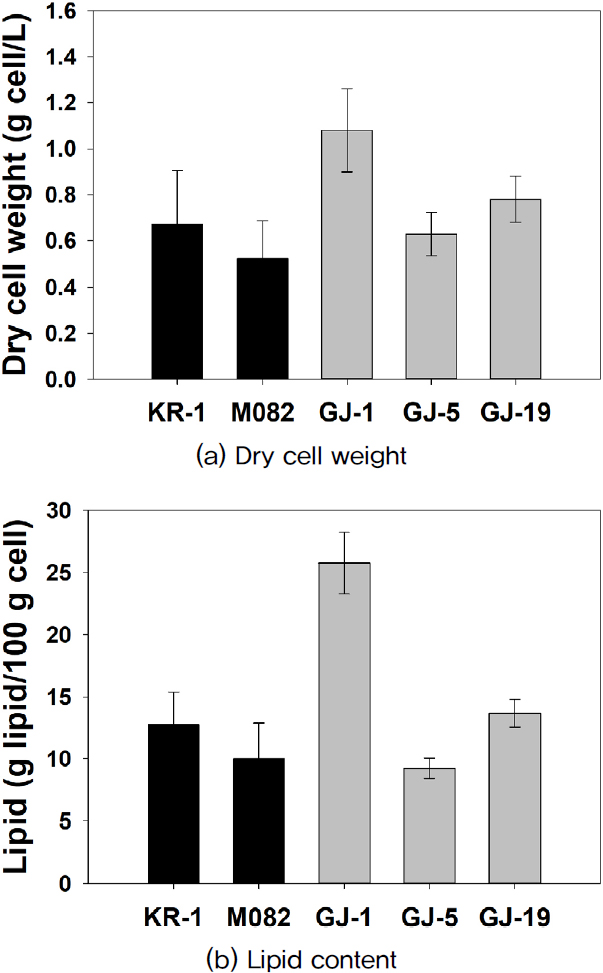
Final dry cell weight and lipid content of selected microalgae and model strains under photosynthetic flask culture condition a t 40°C. The results a re reported as the mean ± S.D. (n=3)
분석 결과, Chlorella sp. KR-1은 건조중량 0.67 g/L, 지질 함량 12.77 g/100 g cell로 M082보다 높은 생산성을 나타내었다. GJ-1은 건조중량 1.08 g/L와 지질 함량 25.74 g/100 g cell로 가장 우수한 값을 나타내었다. GJ-19는 건조중량 0.78 g/L, 지질 함량 13.68 g/100 g cell로 대조군보다 높은 생산성을 보였다. 반면, GJ-5는 건조 중량 0.63 g/L와 지질 함량 9.24 g/100 g cell로 열 내성 균주로 적합하지 않은 것으로 판단되었다.
이 결과를 종합하면, GJ-1은 대조군 및 다른 후보군들에 비해 40°C 환경에서 높은 바이오매스 와 지질 생산량을 보여 열 내성이 우수한 특성을 나타냈으며, 고온 환경에서 활용 가능성이 높은 균주로 평가되었다.
3.3 미세조류 생물학적 동정
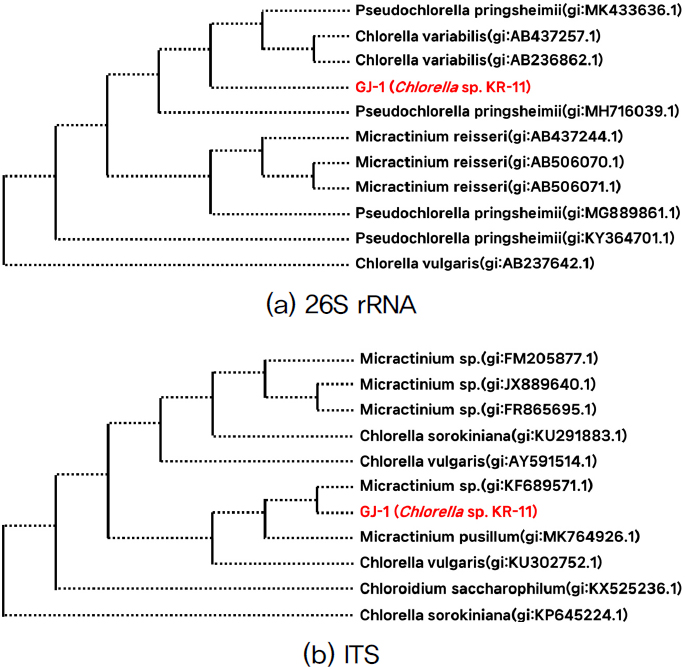
내열성이 우수한 균주로 선정된 GJ-1에 대해 26S rRNA와 ITS 유전자 서열 분석을 통해 생물학적 동정을 수행하였다(Fig. 4 참조).
계통도 분석 결과, GJ-1은 26S rRNA와 ITS 서열에서 각기 다른 유연관계를 나타냈다. 26S rRNA서열(5786 bp) 분석에서는 Pseudochlorella pringsheimii와 유연관계를 보였고, ITS 서열(1379 bp)분석에서는 Micractinium sp.와 더 가까운 유연관계를 보였다. 두 균주는 모두 Chlorellaceae과에 속하는 녹조류로, GJ-1이 이 과의 다양한 종과 연관이 있음을 시사한다. 특히, NCBI 데이터베이스를 활용한 분석 결과, GJ-1의 26S rRNA 유전자 서열은 P. pringsheimii (KY364701.1)와 98.57%의 일치도를, ITS 유전자 서열은 C. sorokiniana(KU291883.1)와 99.53%의 높은 일치도를 보였다.
ITS 유전자 서열의 높은 일치도를 바탕으로, GJ-1은 Chlorella 속에 속하는 것으로 추정되며, 본 연구에서는 이를 Chlorella sp. KR-11(KCTC15029BP)으로 명명하였다.
3.4 온도별 배양 특성
Chlorella sp. KR-11(GJ-1)의 성장을 30°C와 40°C에서 비교한 결과는 Fig. 5(a)에 제시되었다. 배양 14일 후 OD 값은 30°C에서 3.13, 40°C에서 2.07로 확인되었으며, 30°C에서의 OD 값이 40°C 보다 약 1.51배 높게 나타났다.
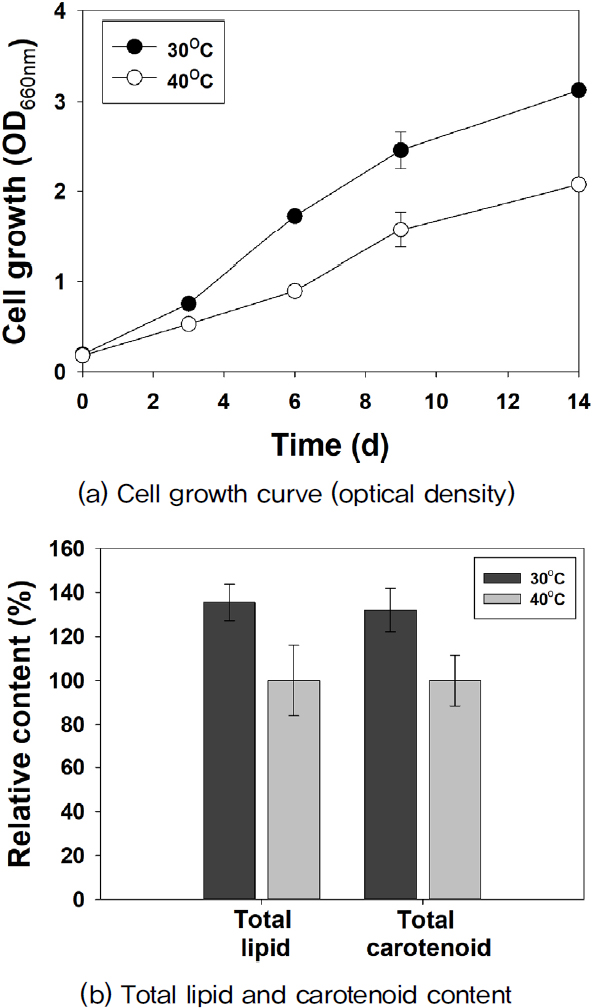
Growth characteristic of Chlorella sp. KR-11 (GJ-1) at 30°C and 40°C. The results are reported as the mean ± S.D. (n=3)
Fig. 5(b)는 총 지질 및 카로티노이드 함량을 비교한 결과를 보여준다. 30°C에서 총 지질 및 카로티노이드 함량은 40°C에 비해 각각 135.5%와 132.1% 더 높게 나타났다. 이러한 차이는 고온(40°C)에서 열에 인한 단백질 변성과 스트레스가 성장뿐만 아니라 지방산 및 색소 생성에 부정적인 영향을 미친 결과로 해석된다.
일반적으로 Chlorella sp.의 최적 성장 온도는 30~35°C로 알려져 있으며, 이 범위를 벗어난 온도에서는 성장이 심각히 저하되고 지방산과 색소 조성에도 큰 변화를 초래한다는 보고가 있다.[2,19] 본 연구에서도 30°C가 Chlorella sp. KR-11 (GJ-1)의 지질 생산과 바이오매스 성장에 최적의 조건임을 확인하였으며, 40°C에서는 생장이 다소 억제되고 대사 활동이 감소하는 경향을 보였다.
미세조류의 지질 내 지방산 조성과 포화 지방산 함량은 바이오연료 생산과 품질에 중요한 영향을 미친다. Fig. 6은 배양 14일 후 수확된 Chlorella sp. KR-11(GJ-1)의 주요 지방산과 카로티노이드 함량을 나타낸다. 주요 지방산으로 Palmitic acid(C16:0), Linoleic acid(C18:2n6c), Linolenic acid(C18:3n3c)가 확인되었다.
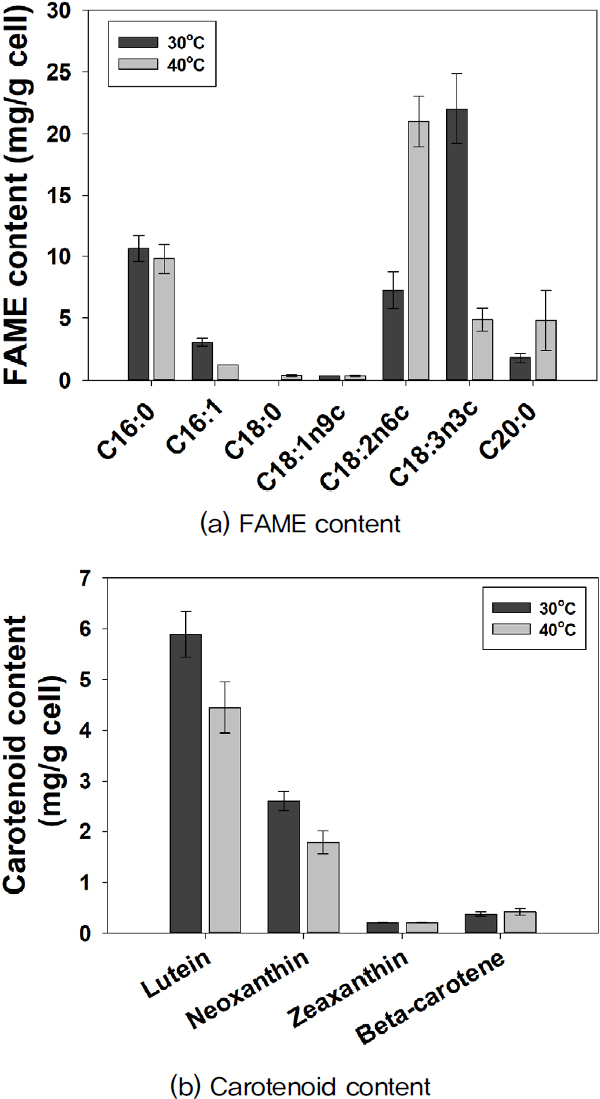
The contents of FAME and carotenoid in Chlorella sp. KR-11 (GJ-1) at 30°C and 40°C. The results are reported as the mean ± S.D. (n=3)
30°C에서는 Linolenic acid(C18:3n3c)가 22.0%로 가장 높은 비율을 보였으나, 40°C에서는 Linoleic acid(C18:2n6c)가 21.0%로 우세했다. 이는 삼중 불포화 지방산이 이중 불포화 지방산으로 전환되는 과정에서 비롯된 것으로 보인다.[2] 이러한 변화는 세포막의 유동성과 안정성 유지에 기인하며, 고온조건에서 Arachidic acid(C20:0)와 같이 장쇄 지방산의 생성 증가도 확인되었다.
Chlorella sp. KR-11(GJ-1)의 카로티노이드 분석 결과, 주요 성분으로 Lutein, Neoxanthin, Zeaxanthin, β-Carotene이 확인되었다(Fig. 6(b) 참조). 이 중 Lutein과 Neoxanthin의 함량이 가장 높게 나타난 반면, Zeaxanthin, β-Carotene은 상대적으로 낮은 함량으로 확인되었다. Fernandes et al.(2020)의 연구에 따르면 C.sorokiniana를 25°C에서 배양하였을 때 Neoxanthin, α-Carotene, β-Carotene, Lutein, Violaxanthin, Zeaxanthin 등 다양한 카로티노이드가 합성되는 것으로 보고되었다.[20] 이는 Chlorella속의 균주가 온도와 배양조건에 따라 다양한 카로티노이드를 합성할 수 있음을 뒷받침한다.
30°C에서는 Lutein과 Neoxanthin이 가장 높은 함량을 보였다. 그러나 40°C에서는 Lutein과 Neoxanthin의 함량이 각각 세포당 1.442 mg/g, 0.814 mg/g 감소하였고, Zeaxanthin과 β-Carotene은 각각 세포당 0.004 mg/g, 0.046 mg/g 증가하는 경향을 보였다. 이는 고온 조건에서 카로티노이드 합성 경로가 조정된 결과로 해석된다.
카로티노이드의 생합성 경로 중 Lycopene을 출발점으로 두 가지로 나뉜다. 첫 번째 경로에서는 LCYE(Lycopene ε-Cyclase) 효소가 Lycopene에 작용하여 δ-Carotene과 α-Carotene을 거쳐 최종적으로 Lutein을 생성하며, 두 번째 경로에서는 LCYB(Lycopene β-Cyclase) 효소가 Lycopene에 작용하여 β-Carotene, Zeaxanthin, Violaxanthin을 거쳐 Neoxanthin을 합성한다.[21]
본 연구 결과, Lutein과 Neoxanthin의 함량 감소와 β-Carotene 및 Zeaxanthin의 함량 증가 경향은 고온에서 LCYE 효소의 활성이 감소하고 LCYB 경로 중간 산물이 축적된 결과로 해석할 수 있다. 이러한 메커니즘은 고온 스트레스에 대한 세포의 적응과정으로 세포막 안정성 유지 및 산화 스트레스 방어를 위한 조절 반응으로 이해된다.
4. 결 론
본 연구에서는 고온 환경에서 성장과 생산성이 우수한 Chlorella sp. KR-11(GJ-1)을 선별하고, 이 균주의 생리적 특성과 생장 패턴을 평가하였다. Chlorella sp. KR-11 (GJ-1)은 건조중량(1.08 g cell/L)과 지질함량(25.74 g/100 g)에서 가장 높은 값을 기록했으며, 고온 조건에서도 대조군에 비해 상대적으로 높은 성장률과 내열성을 유지하였다.
고온(40°C)에서는 바이오매스, 지질, 카로티노이드 함량이 감소하였지만, 포화 지방산 비율 증가와 특정 카로티노이드 중간 산물 축적은 세포막 안정성과 열 내성 강화의 적응 메커니즘으로 해석된다.
이 연구는 고온 환경에서도 높은 생산성을 유지할 수 있는 내열성 미세조류의 가능성을 보여주며, Chlorella sp. KR-11(GJ-1)은 바이오연료 및 고부가가치 색소 생산을 위한 유망한 산업적 후보로 평가된다.[22]
Acknowledgments
본 연구는 환경산업기술원 야생생물 유래 친환경 신소재 및 공정 기술 개발사업(RS-2021-KE001986) 및 한국연구재단 개인기초연구(RS-2024-00337717)의 지원을 받아 수행되었습니다.
References
-
Song, K., Zhou, Z., Huang, Y., Chen, L., and Cong, W., 2023, “Multi-omics insights into the mechanism of the high-temperature tolerance in a thermotolerant Chlorella sorokiniana”, Bioresour. Technol., 390, 129859.
[https://doi.org/10.1016/j.biortech.2023.129859]

-
Barten, R., Djohan, Y., Evers, W., Wijffels, R., and Barbosa, M., 2021, “Towards industrial production of microalgae without temperature control: The effect of diel temperature fluctuations on microalgal physiology”, J. Biotechnol., 336, 56-63.
[https://doi.org/10.1016/j.jbiotec.2021.06.017]

-
Ammar, F.E.B., Saidane, F., Messaoud, C., and Hamdi, M., 2024, “Screening of efficient microalgae strains isolated from Tunisian ecosystems: Assessment of algal growth rate and added-value bioproducts for biorefinery applications”, Biocatal. Agric. Biotechnol., 58, 103140.
[https://doi.org/10.1016/j.bcab.2024.103140]

-
Balasubramaniam, V., Gunasegavan, R.D., Mustar, S., Lee, J.C., and Mohd Noh, M.F., 2021, “Isolation of industrial important bioactive compounds from microalgae”, Molecules, 26(4), 943.
[https://doi.org/10.3390/molecules26040943]

-
Bleeke, F., Rwehumbiza, V.M., Winckelmann, D., and Klöck, G., 2014, “Isolation and characterization of new temperature tolerant microalgal strains for biomass production”, Energies, 7(12), 7847-7856.
[https://doi.org/10.3390/en7127847]

-
Hawrot-Paw, M., and Sąsiadek, M., 2023, “Optimization of microalgal biomass production in vertical tubular photobioreactors”, Energies, 16(5), 2429.
[https://doi.org/10.3390/en16052429]

-
Kato, H., Suzuki, H., Wijffels, R.H., Schulze P.S.C., and Hulatt, C.J., 2024, “Thermal responses of Tetradesmus obliquus for industrial outdoor cultivation”, Bioresour. Technol. Rep., 27, 101909.
[https://doi.org/10.1016/j.biteb.2024.101909]

-
Serra-Maia, R., Bernard, O., Gonçalves, A., Bensalem, S., and Lopes, F., 2016, “Influence of temperature on Chlorella vulgaris growth and mortality rates in a photobioreactor”, Algal Res., 18, 352-359.
[https://doi.org/10.1016/j.algal.2016.06.016]

-
Dai, Y.R., Wang, D., Zhu, Y.R., Yang, K.X., Jiao, N., Sun, Z.L., and Wang, S.K., 2022, “Thermal-tolerant potential of ordinary Chlorella pyrenoidosa and the promotion of cell harvesting by heterotrophic cultivation at high temperature”, Front. Bioeng. Biotechnol., 10, 1072942.
[https://doi.org/10.3389/fbioe.2022.1072942]

-
Barten, R.J.P., Wijffels, R.H., and Barbosa, M.J., 2020, “Bioprospecting and characterization of temperature tolerant microalgae from Bonaire”, Algal Res., 50, 102008.
[https://doi.org/10.1016/j.algal.2020.102008]

-
Barten, R., van Workum, D.J.M., de Bakker, E., Risse, J., Kleisman, M., Navalho, S., Smit, S., Wijffels, R.H., Nijveen, H., and Barbosa, M.J. 2022, “Genetic mechanisms underlying increased microalgal thermotolerance, maximal growth rate, and yield on light following adaptive laboratory evolution”, BMC Biol., 20, 242.
[https://doi.org/10.1186/s12915-022-01431-y]

-
Arora, N., Lo, E., and Philippidis, G.P., 2022, “A two-prong mutagenesis and adaptive evolution strategy to enhance the temperature tolerance and productivity of Nannochloropsis oculata”, Bioresour. Technol., 364, 128101.
[https://doi.org/10.1016/j.biortech.2022.128101]

-
Arora, N., Yen, H.W., and Philippidis, G.P., 2020, “Harnessing the power of mutagenesis and adaptive laboratory evolution for high lipid production by oleaginous microalgae and yeasts”, Sustainability, 12(12), 5125.
[https://doi.org/10.3390/su12125125]

-
Lepage, G., and Roy, C.C., 1984, “Improved recovery of fatty acid through direct transesterification without prior extraction or purification”, J. Lipid Res., 25(12), 1391-1396.
[https://doi.org/10.1016/S0022-2275(20)34457-6]

-
Mahadi, R., Kim, S., Ilhamsyah, D.P.A., Vahisan, L.P.S., Narasimhan, A.L., Park, G.W., Lee, S.Y., and Oh, Y.K., 2023, “Rapid accumulation of astaxanthin in Haematococcus pluvialis induced by mild hydrostatic pressure”, Biotechnol. Bioprocess Eng., 28, 345-351.
[https://doi.org/10.1007/s12257-023-0017-4]

- Lee, J.S., Sung, K.D., Park, S.C., Choi, M.J., and Lee, K.W., 2000, “A highly CO2 tolerant Chlorellasp. KR-1 and CO2 fixation technology using Chlorellasp. KR-1”, KR Patent No. 1002650340000.
- Oh, Y.K., Park, J.Y, Lee, J.S., Park, S.C., Kim, D.K., Lee, J.P., Kim, B.H., and Choi, E.J., 2013, “Chlorella sp. M082 having excellent carbon dioxide fixation ability at high temperature and uses thereof”, KR Patent No. 10127323 40000.
-
Duong, V.T., Ahmed, F., Thomas-Hall, S.R., Quigley, S., Nowak, E., and Schenk, P.M., 2015, “High protein- and high lipid-producing microalgae from northern Australia as potential feedstock for animal feed and biodiesel”, Front. Bioeng. Biotechnol., 3, 53.
[https://doi.org/10.3389/fbioe.2015.00053]

-
Choi, Y.Y., Hong, M.E., Chang, W.S., and Sim, S.J., 2019, “Autotrophic biodiesel production from the thermotolerant microalga Chlorella sorokiniana by enhancing the carbon availability with temperature adjustment”, Biotechnol. Bioprocess Eng., 24(1), 223-231.
[https://doi.org/10.1007/s12257-018-0375-5]

-
Fernandes, A.S., Petry, F.C., Mercadante, A.Z., Jacob-lopes, E., and Zepka, L.Q., 2020, “HPLC-PDA-MS/MS as a strategy to characterize and quantify natural pigments from microalgae”, Curr. Res. Food Sci., 3, 100-112.
[https://doi.org/10.1016/j.crfs.2020.03.009]

-
Lou, S., Lin, X., Liu, C., Anwar, M., Li, H., and Hu, Z., 2021, “Molecular cloning and functional characterization of CvLCYE, a key enzyme in lutein synthesis pathway in Chlorella vulgaris”, Algal Res., 55, 102246.
[https://doi.org/10.1016/j.algal.2021.102246]

-
An, S., Lee, N., Park, J., Kim, Y.E., Jung, M., Kim, J., and Oh, Y.K., 2024, “Long-term photosynthetic Chlorella cultivation in recycled medium for sustainable lipid production”, New. Renew. Energy, 20(4), 38-46.
[https://doi.org/10.7849/ksnre.2024.0027]