Online publication date 25 Mar 2025
플라스틱 및 바이오매스의 열중량 분석 및 열분해 반응속도론에 관한 연구
© 2025 by the New & Renewable Energy
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Carbon neutrality is the balance between carbon emission and absorption from the soil, forest, and oceans. A variety of renewable energy sources, such as solar, wind, hydrogen, biomass energy, and waste energy, have been studied worldwide to achieve carbon neutrality by 2025. In particular, pyrolytic oil produced from plastic and biomass is considered a promising energy for achieving carbon neutrality because it can be effectively used not only for heat transfer but also as transport fuel. Furthermore, pyrolytic oil produced from plastics has been used as a feedstock in chemical processes to produce sustainable monomers and chemicals. However, most plants used for producing pyrolytic oil have been built in batch, not continuous manufacturing. Therefore, it is essential to scrutinize the thermal decomposition characteristics of plastics and biomass to build commercial plants. In this study, to discover the kinetic parameters and dynamic thermogravimetric characteristics, the thermal degradation of 3 types of plastics (LDPE, HDPE, PP) and sawdust was examined using a TGA under a nitrogen atmosphere of isothermal conditions in the range of 375°C, 400°C, 425°C, and 450°C. The results showed that the calculated activation energy was LDPE 136.11 kJ/mol, HDPE 181.99 kJ/mol, PP 149.39 kJ/mol, and Sawdust 34.73 kJ/mol.
Keywords:
Plastics, Sawdust, Kinetic analysis, Activation energy키워드:
플라스틱, 톱밥, 반응속도론 연구, 활성화에너지1. 서 론
지구 온난화로 인한 기후 상승은 농작물 생산 감소, 산림지대 감소, 해수면 상승, 기상이변, 대기오염 악화 등의 피해를 발생시키고 있다. 1970년대에 들어서면서 인간의 활동으로 인한 온실가스 배출이 지구 온난화를 초래한다는 논의가 이루어졌으며, 기후변화에 대한 과학적 근거를 제시하기 위해 1988년 유엔환경계획(UNEP)과 세계기상기구(WMO)는 ‘기후변화에 관한 정부간협의체’(Intergovernmental Panel on Climate Change, IPCC)를 설립하였다. 1992년 국제사회는 IPCC의 보고서를 바탕으로 ‘유엔기후변화협약(UN Framework Convention on Climate Change, UNFCCC)을 채택하였으며, 이후 1997년 교토의정서(Kyoto Protocol)와 2015년 파리협정(Paris Agreement)을 연달아 채택 함으로써 지구 온난화 방지를 위한 대책을 명문화하였다. 특히 파리협정에서는 총 195개국의 선진국과 개발도상국이 참여 하여 산업화 이전과 대비하여 지구 평균기온 상승을 2°C보다 상당히 낮은 수준으로 유지하고, 1.5°C 이내로 제한하기 위한 노력을 추구한다는 구체적인 목표를 제시하였다.[1~3]
이러한 기조 아래 국제사회는 2019년 9월 지구 온난화를 막기 위한 ‘기후 행동 정상회의(UN Climate Summit)’에서 65개국 정상들이 2050년 탄소중립 달성을 선언하였으며, 세계적인 탈산소 정책 강화에 따라 우리나라 역시 2021년 10월 2030 국가 온실가스 감축목표(NDC) 상향안 및 2050 탄소중립 시나리오를 발표하였다. 같은 해 12월에는 에너지 공급, 산업, 수송, 건물, 폐기물 등을 포함한 한국형(K)-순환 경제 이행계획을 수립하였다. 특히, 계획안에는 플라스틱 사용의 급증에 따른 다양한 사회적 문제가 발생함에 따라 폐플라스틱의 사용을 획기적으로 감축할 수 있는 전략이 필요하며, 폐기물의 열분해 분야에서 기존에 주로 연료로 활용하던 열분해유를 석유·화학 공정의 원료로 사용할 수 있도록 하였다. 또한 석유화학 기업이 원유를 대체하여 열분해유를 납사, 경유 등 석유 제품으로 재활용할 수 있도록 관련 지침을 변경하고, 폐플라스틱 열분해 처리 비중을 2020년 0.1%에서 2030년 10%까지 확대하는 내용을 포함하고 있어 관련 산업의 수요가 높아질 전망이다.[4,5]
열분해 기술이란 고분자 폐기물을 무산소 분위기에서 가열하여 분자를 구성하는 탄소 사슬을 끊고 작은 저분자로 만들어 주는 기술이다. 또한 열분해 기술은 열전달 속도 및 반응기 체류 시간에 따라 저속 열분해(Slow Pyrolysis), 급속 열분해(Fast Pyrolysis)로 구별할 수 있으며, 바이오매스를 액체연료(바이오원유)로 전환하기 위한 목적으로 급속 열분해 기술이 많이 이용되고 있다. 앞서 설명한 바와 같이 최근에는 탄소중립 정책에 따른 폐플라스틱의 자원순환 생태계 구축에 대한 요구가 증가하고 있어, 바이오원유 생산뿐만 아니라 폐플라스틱의 열분해유 생산에 대한 관심도 높아지고 있다.[6~8] 하지만 바이오매스 및 폐플라스틱의 연속식 열분해 설비는 아직까지 상용화 사례가 없어 이러한 고분자 화합물에 대한 기초적인 열분해 특성 및 반응속도론 연구는 최적의 열분해 반응기 설계를 위한 필수 연구분야라고 할 수 있다.[9,10]
TGA 장비는 질소분위기에서 가열에 의한 시료의 무게변화를 측정하여 반응속도상수 계산을 위한 기초 데이터를 제공하는 장치로써 가열속도 및 열분해 온도의 제어가 용이하여 널리 이용되고 있다. 이러한 장점으로 인해 TGA 장비를 이용한 고분자 화합물의 반응속도론 연구는 다양하게 수행되고 있지만, 대부분의 연구가 가열속도에 변화를 주어 반응속도상수를 계산하는 모델을 많이 사용하고 있다. 하지만 실제 열분해 설비에서는 반응온도를 고정하고 열분해가 수행되기 때문에, 등온과정에서의 kinetic 연구 또한 반드시 필요하다고 할 수 있다. 본 연구에서는 3종의 플라스틱(LDPE, HDPE, PP)과 Sawdust를 375~450°C의 등온과정에서 열분해하고, 기초데이터를 바탕으로 열중량 분석 및 Kinetic 연구를 수행하여 각 결과를 비교 검토하였다.
2. 실험 장치 및 방법
2.1 시료
열중량 분석을 위한 시료는 Fig. 1과 같이 3종의 LDPE, HDPE, PP의 플라스틱과 Sawdust를 사용하였으며, 각 시료의 열중량 분석의 균질성을 위해 시료를 분쇄하여 입자 크기 1 mm로 동일하게 하였다. Table 1은 각 시료의 물성 분석 결과를 나타내고 있다. 3종의 플라스틱의 경우 고위발열량 측정값은 LDPE는 11034.85 kcal/kg, HDPE는 11197.25 kcal/kg, PP는 11104.75 kcal/kg으로 나타났으며, 톱밥의 경우는 4231.2 kcal/kg을 보였다. 또한 각 시료의 원소분석 결과 3종의 플라스틱의 경우 전체적으로 탄소와 수소의 함량이 약 85%와 14%로 측정되었다. 질소는 약 0.18%, 산소 및 황의 함량은 존재하지 않는 것으로 나타났으며, 대부분 탄소와 수소만으로 이루어져 있음을 확인할 수 있다. 톱밥의 경우 탄소 함량은 약 44%로 낮게 측정되었으며, 그에 비해 산소 함량은 50.78%로 높은 함량을 보였다. 이러한 바이오매스의 높은 산소 함량은 바이오매스에서 전환된 바이오원유가 낮은 발열량을 가지는 원인이 되는 것으로 알려져 있다.[11]
2.2 Kinetics
Fig. 2는 TGA 701 LECO로 반응속도론 연구를 위한 장비이다. 본 장비를 이용하여 분석 데이터를 측정하였으며, 측정된 데이터를 이용하여 반응속도 상수인자 및 활성화에너지를 계산하였다. 플라스틱 3종(LDPE, HDPE, PP) 및 Sawdust의 약 0.5 g을 세라믹 도가니에 담고 질소분위기에서 시료를 열분해하였다. Table 2는 본 연구에서의 실험 조건을 나타내고 있다. 열분해 기술은 목표로 하는 최종 생성물에 따라 열분해 온도를 다르게 적용하는데 바이오매스를 액상의 생성물로 전환하기 위해서는 열분해 온도를 450~550°C로 설정하며, 450°C 이하의 온도에서는 Char, 600°C 이상의 온도에서는 가스 생산을 목적으로 한다.[7] 플라스틱의 경우도 열분해 온도에 따라 최종 생성물의 차이를 가져올 수 있으므로, 각 물질의 열분해 특성을 정확하게 파악하기 위해서는 다양한 온도 조건에서 실험이 필요하다. 그러므로 본 실험에서는 비교적 낮은 온도인 375°C를 초기 조건으로 설정하였으며, 25°C씩 온도를 상승시키면서 450°C까지 실험을 수행하였다. 또한 승온속도를 최대한 빠르게 하여 반응온도까지 도달하는 시간을 최소화하였다.
450°C의 30°C/min 기준으로 각 반응온도에 도달하는 시간을 15 min으로 고정하였다. 이후 실제 열분해 과정에서 이루어지는 현상과 동일한 조건에서 시료의 열분해 데이터를 획득하기 위해 각 반응온도를 고정하고 일정 시간 동안 유지하였다. 특히, 반응온도 375°C의 경우 PP를 제외한 모든 시료에서 온도 유지 시간을 12 hr를 유지하여 최대한 열분해 되도록 하였는데 자세한 내용은 열중량 분석에서 논의 될 예정이다.
열분해 반응속도 공식을 정의하면 식 (1)과 같다.[12,13]
| (1) |
여기에서 t는 시간이며, K(T)는 온도 함수인 Arrhenius 속도상수, T는 절대 온도 (K), f(α)는 시간에 따라 아직 반응하지 시료의 농도이다. f(α)를 정의하면 식 (2)와 같다.
| (2) |
여기에서 n은 반응차수로 기존 다수의 실험에서 1로 가정하여 해석하고 있으며, 본 실험에서도 1로 하였다.[14~16] α(0≤α≤1)는 열분해 전환율로 식을 정의하면 다음 식 (3)과 같다.
| (3) |
mi는 초기 시료 무게, m시간에 따른 남은 시료의 무게, mf는 열분해 완료 후 남은 최종 시료 무게를 의미한다. 따라서 열분해 시작 전에는f(α)=1, 열분해 종료 후에는 f(α)=0 이 된다. k(T)를 구하기 위해 식 (1)에 식 (2)를 대입하면 다음 식 (4)와 같다.
| (4) |
식 (4)의 양변을 적분하면 다음 식 (5)의 공식을 얻을 수 있다.
| (5) |
식 (3)을 이용하여 α값을 구한 후, 식 (5)에 대입하여 선형회귀 하면 Y=aX+b 형태의 직선방정식을 구할 수 있다. 여기에서 기울기 값인 a=k(T)이므로, k(T)값을 구할 수 있으며, 식 (6)과 같이 정의할 수 있다.
| (6) |
여기에서 A는 빈도인자(min-1), Ea는 활성화에너지(kJ/mol), R은 일반기체상수(8.3145×10-3 kJ/mol·K)이다. 위 식을 양변을 적분하여 변형하면 식 (7)을 얻을 수 있다.
| (7) |
식 (5)를 이용하여 각 열분해 온도에 대한 k(T)를 구한 후, 식 (7)에 대입하면 Y=aX-1+b 형태의 직선 방정식을 도출할 수 있다. 여기에서 기울기인 a=-Ea/R과, y절편인 b=InA를 이용하면 최종적으로 각 시료에 대한 활성화에너지 및 빈도인자를 구할 수 있다.
3. 실험 결과
3.1 열중량 분석
Fig. 3은 LDPE의 시간에 따른 열분해 전환율, 시료 무게 변화량, 열분해 속도(DTG curve) 결과를 보여 준다. 앞서 설명한 바와 같이 실제 열분해 조건에 부합하기 위해 등온과정으로 실험을 수행하였으며, 열분해 온도에 도달하는 시간을 최대한 빠르게 하고 설정한 열분해 온도에 도달하면 일정 시간 동안 온도를 유지하여 시료가 최대한 열분해 될 수 있도록 하였다. LDPE의 경우는 전체적으로 온도가 높아질수록 열분해가 빠르게 진행되는 것을 확인할 수 있으며, 425°C, 450°C의 경우 승온시간 이후 시료가 분해되기 시작하여 전환율이 95%까지 분해되는 시간은 약 75 min, 20 min이 소요되었다. 375°C, 400°C의 경우 시료가 오랜 시간 천천히 분해되는 현상이 관찰되었으며, 400°C에서는 290 min이 소요되어 450°C와 비교했을 때 10배 이상의 시간이 소요되는 것을 확인할 수 있다. 특히, 375°C의 경우는 Fig. 3(b)와 같이 약 12 hr의 온도 유지 후에도 9%의 잔여물이 남아 시료가 완전히 열분해 되지 않았음을 확인할 수 있다. Fig. 3(c)는 각 시료의 DTG curve를 나타내며, 각 온도에서 시료의 열분해 속도를 정량적으로 확인할 수 있다. 그래프를 보면 375°C와 400°C에서는 열분해 속도가 거의 완만하게 진행되다가, 425°C에서 열분해 속도가 증가하기 시작하여 450°C에서 가장 높은 열분해 속도를 보였다. 이러한 현상은 선행 문헌에서도 확인할 수 있는데 LDPE의 경우 열분해 속도가 온도에 굉장히 민감하게 작용하는 것을 확인할 수 있으며, 425°C 이상의 온도에서 활발한 열분해가 일어남을 알 수 있다.[13]
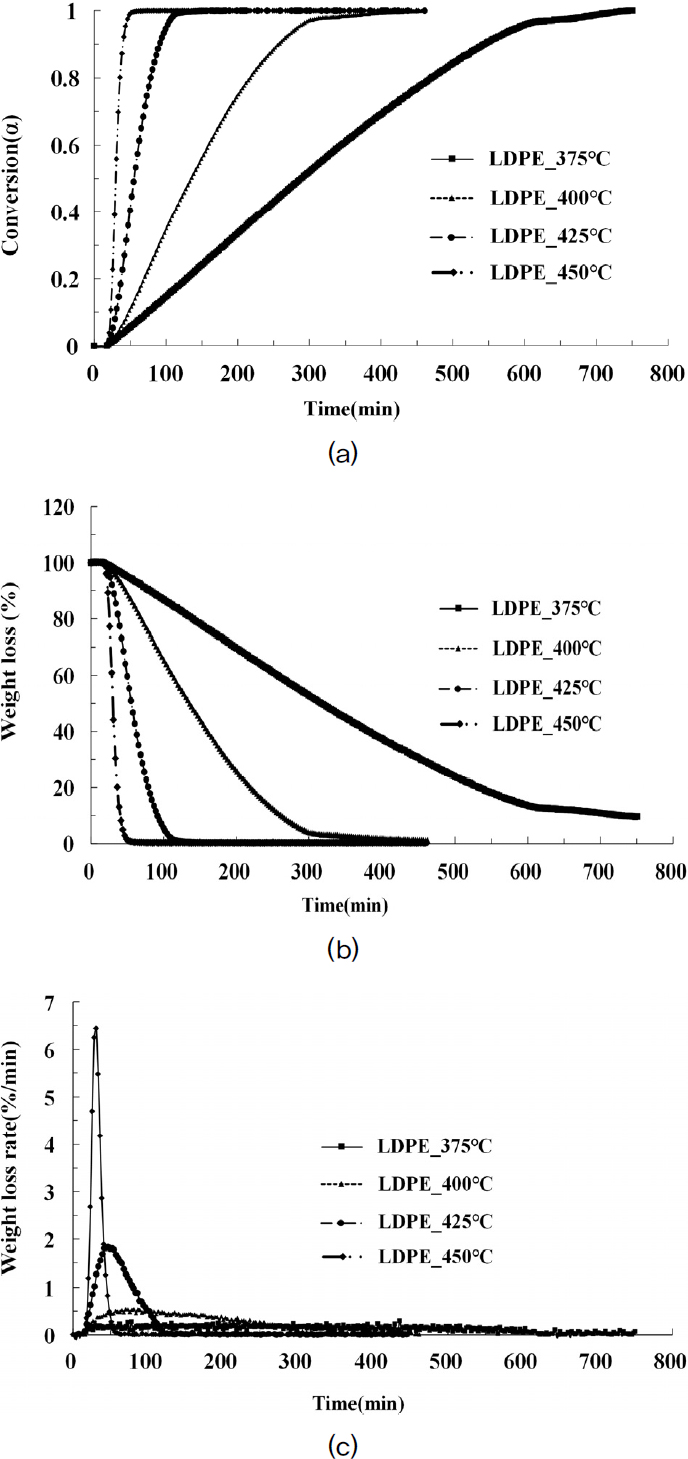
(a) Conversion (α) versus time, (b) Weight loss (%) versus time and (c) Weight loss rate (%/min) versus time (Low density polyethylene)
Fig. 4는 HDPE의 시간에 따른 열분해 전환율, 시료 무게 변화량, 열분해 속도(DTG curve) 결과를 보여 준다. Fig. 4(a)를 보면 HDPE 역시 온도가 높아질수록 열분해가 빠르게 진행되는 것을 확인 할 수 있으며, 425°C, 450°C에서 시료의 전환율이 95%까지 소요 되는 시간은 80 min, 20 min으로 LDPE의 분해 시간과 거의 비슷하였다. 하지만 400°C의 경우 약 300 min 소요되어 HDPE 역시 열분해 속도에 온도가 굉장히 민감하게 작용함을 알 수 있다. Fig. 4(b)와 같이 375°C에서는 반응시간 12 hr 이후에도 15%의 잔여물이 남는 것을 확인할 수 있었으며, 이것은 400°C 이하의 온도에서는 LDPE에 비해 열분해 속도가 느릴 뿐만 아니라 최종 열분해의 양도 적은 것을 알 수 있다. 폴리올레핀의 열 안전성은 분자 구조상의 분지에 크게 영향을 받는 것으로 알려져 있는데, LDPE의 분자 구조를 보면 짧은 사슬과 긴 사슬의 분지가 매우 많아 사슬의 결정 구조가 약하지만, HDPE는 분지가 거의 없고 50만~100만 개의 탄소 단위로 구성된 폴리머 사슬로서 결정질 영역의 비중이 많은 것으로 알려져 있다. 그러므로 HDPE는 LDPE보다 단단한 구조를 가지며 열에너지에 강하기 때문에 낮은 온도에서는 열분해가 원활하게 이루어지지 않은 것으로 사료된다.[17,18]
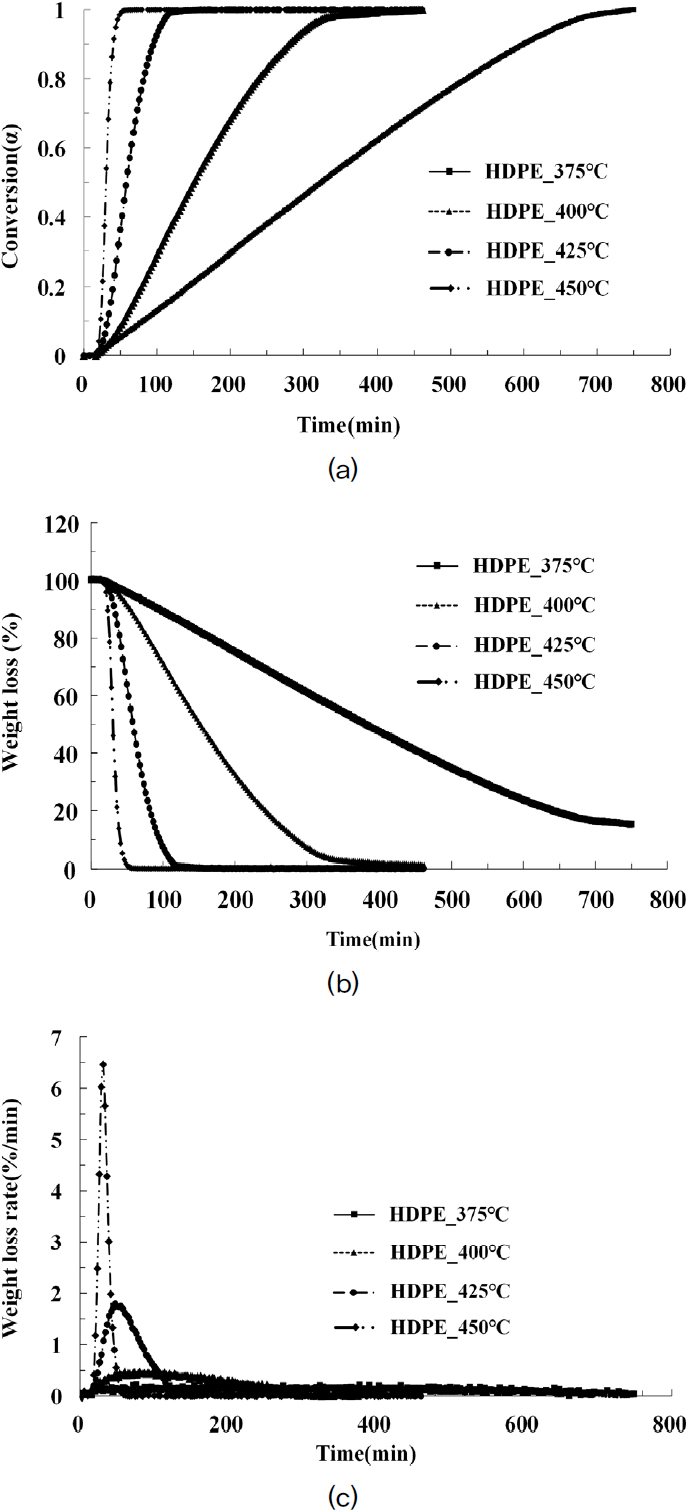
(a) Conversion (α) versus time, (b) Weight loss (%) versus time and (c) Weight loss rate (%/min) versus time (High density polyethylene)
Fig. 5는 PP의 시간에 따른 열분해 전환율, 시료 무게 변화량, 열분해 속도(DTG curve)결과를 보여 준다. PP 역시 Fig. 5(a), (b)에서 알 수 있듯이 온도가 높아질수록 열분해가 빠르게 진행되었으며, 375°C에서도 열분해가 완료되어 LDPE와 HDPE와는 다르게 낮은 온도에서도 열분해가 원활하게 이루어졌다. 각 온도별 전환율 95% 이상까지 소요되는 시간은 375°C, 400°C, 425°C, 450°C에서 160 min, 60 min, 25 min, 15 min으로 3종의 플라스틱 중 가장 빠른 열분해 시간을 보였다.
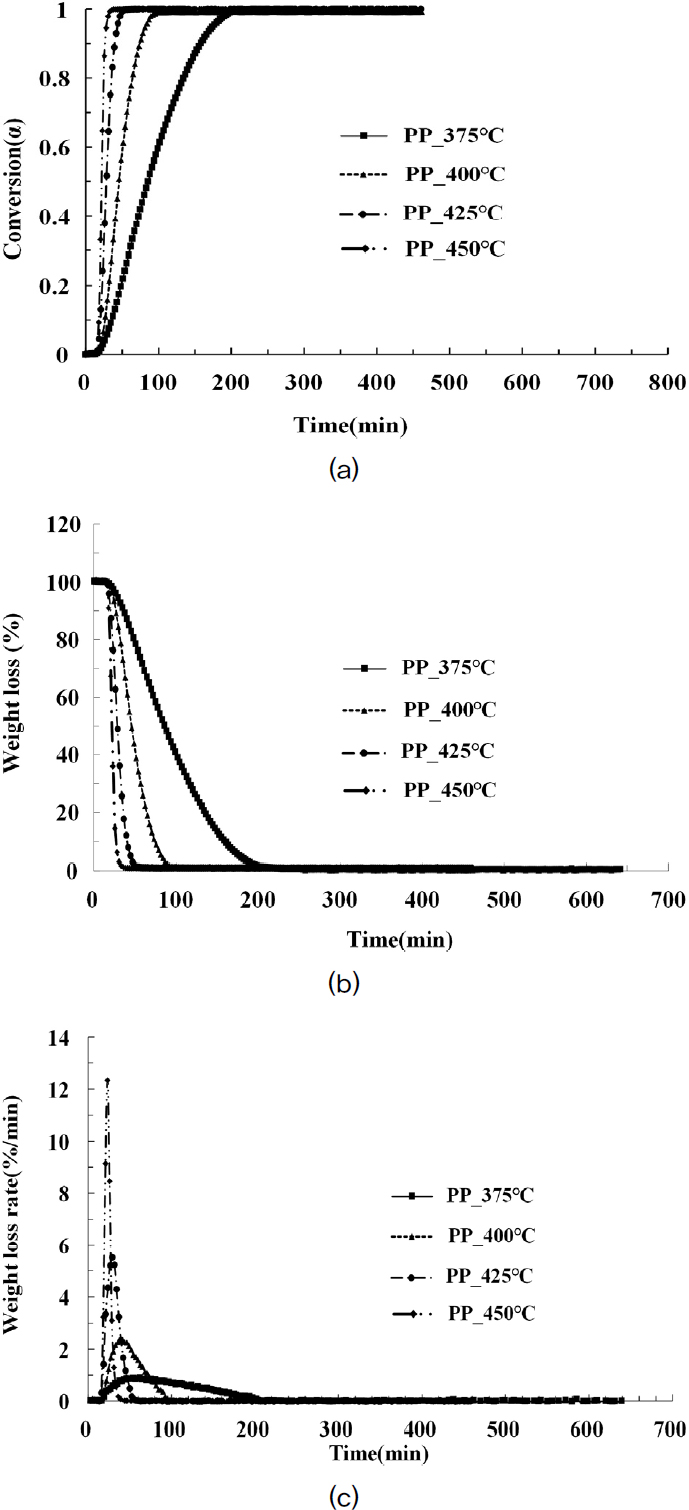
(a) Conversion (α) versus time, (b) Weight loss (%) versus time and (c) Weight loss rate (%/min) versus time (Polypropylene)
또한 Fig. 5(c)를 보면, LDPE와 HDPE와는 다르게 400°C 이하의 온도에서도 선명한 Peak 점을 확인할 수 있는데, PP가 상대적으로 낮은 온도에서도 빠르게 분해 됨을 명확히 확인할 수 있다. 이것은 PP의 경우 주요 폴리머 사슬의 탄소 원자는 Tertiary Carbon으로 이루어져 있는데, Tertiary Carbon은 열 및 촉매 반응에 매우 반응성이 높은 것으로 알려져 있어, LDPE, HDPE이 비해 낮은 온도에서도 열분해가 원활하게 이루어졌음을 알 수 있다.[19]
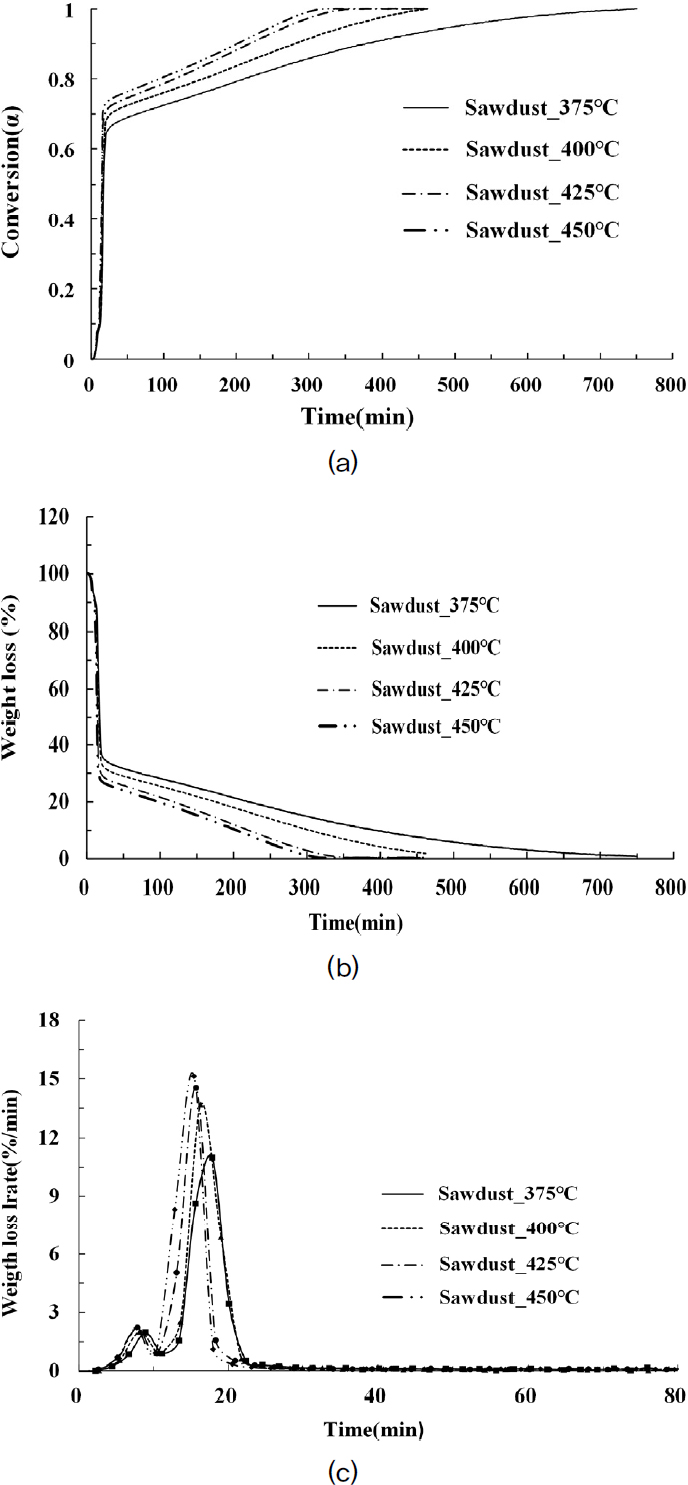
Fig. 6은 Sawdust의 시간에 따른 열분해 전환율, 시료 무게 변화량, 열분해 속도(DTG curve)결과를 보여 준다. Sawdust의 경우 Fig. 6(a), (b)와 같이, 두 구간(1st step, 2nd step)으로 나뉘어 열분해가 일어나는 것을 확인할 수 있다. 플라스틱의 경우 실험 온도에 도달 후 시료가 분해되기 시작하지만, Sawdust의 경우 전체 실험 온도에서 약 200°C부터 빠르게 시료가 분해되기 시작하여 65%까지 분해되는 소요 시간은 평균 10 min 내외로 PP가 95%의 전환율을 보이는 시간과 비슷하였다. 이후 시료는 천천히 분해되어 전환율 95%까지 분해되는데 375°C, 400°C, 425°C, 450°C에서 500 min, 350 min, 254 min, 263 min으로 플라스틱보다 상당히 많은 시간이 필요하였다. 또한 Fig. 3(c)을 보면, 각 실험 온도별 두 개의 Peak이 보이는데, 첫 번째 Peak은 200°C 부근에서, 두 번째 Peak은 370~430°C 사이에서 발생하였다. 이러한 현상은 목질계 바이오매스의 열분해 특성에서 알 수 있는데, 헤미셀룰로스의 열분해 온도는 220~315°C에서 발생하며, 셀룰로스는 315~400°C, 리그닌은 400°C 이상의 온도에서 열분해 되는 것으로 알려져 있다. 그러므로 열분해 온도에 도달하는 과정에서 헤미셀룰로스와 셀룰로스가 먼저 빠르게 분해된 후 리그닌이 천천히 분해 되는 과정을 거치게 되는 것으로 사료 된다.[20,21]
3.2 Kinetic 분석
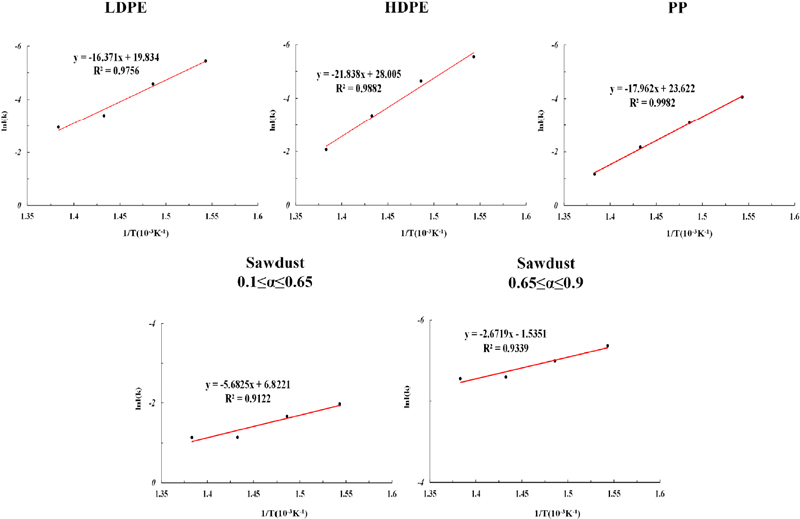
Table 3은 식 (3)과 (5)를 이용하여 계산된 각시료별 k 값 및 R2값을 보여 준다. 식 (3)의 α 값의 범위는 초기 승온 과정에서 필연적으로 발생할 수 있는 오차를 보정 하기 위해 전환율 0.1부터 시작하여, 90%까지 분해되는 구간인 0.9까지(0.1≤α≤0.9)로 설정하였다. Sawdust의 경우는 앞서 설명한 바와 같이 시료의 열분해 구간이 Two steps으로 나뉘게 되며, α값의 영역을 0.1≤α≤0.65, 0.65≤α≤0.9로 구분하여 k 값을 계산하였다.
Table 3을 보면 선형회귀 후 R2값이 높은 것을 확인할 수 있는데, 이것은 높은 수준의 직선성을 확보했음을 보여 준다. 또한 각 시료의 반응속도상수(k) 값은 온도가 높아질수록 증가하는 것을 확인할 수 있다. 본 결과를 바탕으로, k 값을 식 (7)에 대입하여 온도에 따른 ln(k) 값을 구한 후 선형회귀하면 각 시료의 활성화에너지 및 빈도인자를 계산할 수 있다.
그 결과를 Fig. 7과 Table 4에 나타내었다. Fig. 7을 보면, 플라스틱의 경우 R2값이 0.98 이상으로 높은 정확도를 보였다. Sawdust의 1st step의 경우는 0.91, 2nd step의 경우 0.93으로 플라스틱과 비교하여 조금은 낮은 정확도를 보였지만 전체적으로는 0.9 이상의 직선성을 보였다. Table 4을 보면 Fig. 7의 기울기 및 y절편 값을 이용하여 계산된 활성화에너지 및 빈도인자를 나타내고 있다. 플라스틱의 경우 LDPE, HDPE, PP의 활성화에너지가 136.11, 181.99, 149.39 kJ/mol을 나타내었다. HDPE의 활성화에너지가 가장 높게 나타났으며, LDPE가 가장 낮은 수치를 보이는데, 앞서 설명한 바와 같이 폴리올레핀 경우 분자 구조의 차이로 인한 활성화에너지의 차이가 발생함을 알 수 있다. Kim et al.(1999)[9]은 가열속도를 다르게 하여 미분법 및 적분법을 활용한 플라스틱의 Kinetic 연구를 수행하였다. 연구 결과, 미분법에서는 Kissinger 방법이 적분법에서는 Ozawa 방법이 가장 타당하다고 하였는데, Kissinger 방법의 경우 LDPE의 활성화에너지는 191.4 kJ/mol, HDPE의 경우 253.2 kJ/mol을 보이며 본 실험과는 조금 높은 수치를 보였지만 HDPE의 활성화에너지가 높게 나타나는 현상은 동일하였다. 또한 Ozawa 방법의 경우 LDPE의 활성화에너지는 125.2~202.8 kJ/mol, HDPE는 201.4~257.6 kJ/mol로 본 실험의 결과 값을 포함하는 수치를 보였다. Encinar and González(2008)[13]도 같은 연구를 진행하였으며 본 실험과 같이 등온과정에서의 Kinetic 실험을 수행하였다. 실험 결과, LDPE의 경우 활성화에너지는 285.74 kJ/mol, 빈도인자는 2.3×1018, PP 경우 활성화에너지는 169.35 kJ/mol, 빈도인자는 1.06×1010으로 나타났다. PP의 활성화에너지 값은 본 실험 결과와 유사한 수치를 보였지만, LDPE의 활성화에너지는 본 실험 결과 값보다 높게 나타났다. 그 이유는 Encinar의 실험에서는 최대 열분해 온도를 475°C까지 높게 설정하면서, 온도에 민감하게 반응하는 LDPE의 경우 수치의 차이가 보인 것으로 사료된다.[13]
Sawdust의 경우 1st step에서의 활성화에너지는 47.24 kJ/mol로 나타났으며, 2nd step에서는 22.21 kJ/mol로 상대적으로 낮은 수치를 보였다. 이 수치는 평균 34.73 kJ/mol이며, 열분해 중량 변화가 크게 나타난 1st step에서 활성화에너지가 높게 나타났다. 또한 Vitázek et al.(2021)의 연구 결과에 따르면, 등온과정에서의 Wood Chip 시료의 활성화에너지는 34±3 kJ/mol로 본 실험의 평균 활성화에너지 값과 비슷한 수치를 보였다.[12]
4. 결 론
본 연구에서는 TGA 장비를 이용하여 열분해 온도 375~450°C의 등온과정에서 3종의 플라스틱(LDPE, HDPE, PP)과 바이오매스(Sawdust)의 열중량 분석 및 반응속도론에 관한 실험을 수행하였으며, 그 결과는 다음과 같이 요약할 수 있다.
- 1) 열중량 분석 결과, 3종의 플라스틱 및 Sawdust에서 반응 온도가 증가할수록 열분해가 빠르게 진행됨을 확인하였다. LDPE, HDPE의 경우 375°C에서 12 hr의 열분해 시간에도 완전 열분해 되지 못하고 잔여물을 남겼으며, 열분해 시간이 온도에 굉장히 민감하게 작용함을 확인할 수 있었다. PP의 경우 375°C에도 완전 열분해 되었으며, 열분해 시간도 다른 플라스틱에 비해 짧은 것을 확인하였다. 이것은 폴리올레핀의 분자 구조에 기인한 것으로 사료 된다. Sawdust의 경우, 플라스틱과는 다르게 Two steps로 나뉘어 열분해가 진행되었으며, 열분해가 빠르게 진행되는 1st step과 천천히 분해되는 2nd step으로 나뉘었다. 모든 반응 온도에서 1st step이 완료되는 열분해 시간은 약 10 min 소요 되었으며, 열분해 전환율은 65%로 나타났다. 이후 천천히 분해 되는 과정을 거치게 되며, 특히 375°C의 경우 완전 열분해 되는 시간은 750 min이 소요 되었다. DTG curve에서 두 개의 peak이 관찰되었으며, 이것은 목질계 바이오매스를 구성하고 있는 헤미셀룰로스와 셀룰로스의 열분해 특성에 기인한 것으로 사료 된다.
- 2) Arrhenius 속도방정식을 이용하여 활성화에너지 및 빈도인자를 계산하였다. 플라스틱의 경우 열분해 전환율 α를 0.1≤α≤0.9로 설정하여 계산된 LDPE의 활성화에너지는 136.11 kJ/mol, HDPE는 181.99 kJ/mol, PP는 149.32 kJ/mol로 나타났다. Sawdust의 경우 열중량 분석 결과에 따라 열분해 전환율 α를 Two steps으로 나누었으며, 0.1≤α≤0.65, 0.65≤α≤0.9로 하였다. 1st step의 활성화에너지는 47.24 kJ/mol, 2nd step에서는 22.21 kJ/mol로 나타났으며, 평균 활성화에너지는 34.73 kJ/mol을 보였다.
Acknowledgments
본 연구는 2024년 중소벤처기업부의 “연속 투입과 배출이 가능하고 폐수와 미세먼지 발생이 없는 폐플라스틱 열분해 유화 공정 개발”(과제번호: S3264002)의 일환으로 수행되었으며 이에 감사드립니다.
References
- Kim, H.S., 2008, “International cooperation on climate change”, Seoul Peace Prize Cultural Foundation, 5(1), 67-99.
- Chung, S.O., 2009, “Introduction to the climate change research”, Korean National Committee on Irrigation and Drainage, 16(1), 4-10.
-
Park, S.W., 2016, “Post-2020 climate regime and Paris agreement”, Environ. Law Policy, 16, 285-322.
[https://doi.org/10.18215/envlp.16..201602.285]

-
Cheon, Y.H., 2022, “Review of global carbon neutral strategies and technologies”, J. Korean Soc. Miner. Energy Resour. Eng., 59(1), 99-112.
[https://doi.org/10.32390/ksmer.2022.59.1.099]

- Jo, J.H., Sin, D.W., and Kim, Y.H, 2022, “Pyrolysis of plastic waste : Current status and policy tasks”, Korea Environment Institute (KEI), https://scienceon.kisti.re.kr/commons/util/originalView.do?cn=TRKO202300028718&dbt=TRKO&rn=, .
- Shin, D.H, Yun, W.L., and Choi, I.S., 2002, “Chemical recycling of plastic waste and pyrolysis technologies for oil production”, Polym. Sci. Technol., 13(3), 322-331.
- Lee, I.G., and Hwang, K.R., 2012, “Production of bio-oil from lignocellulosic biomass by fast pyrolysis”, Korean Industiral Chemistry NEWS, 15(6), 28-38.
-
Bridgwater, A.V., Meier, D., and Radlein, D., 1999, “An overview of fast pyrolysis of biomass”, Org. Geochem., 30(12), 1479-1493.
[https://doi.org/10.1016/S0146-6380(99)00120-5]

- Kim, M.S., Oh, S.C., Lee, H.P., Kim, H.T., and Yoo, K.O., 1999, “A study on the kinetics of thermal degradation of polyethylene”, Appl. Chem. Eng., 10(4), 548-556.
-
Jeong, Y.W., Choi, S.K., Choi, Y.S., and Kim, S.J., 2015, “Production of biocrude-oil from swine manure by fast pyrolysis and analysis of its characteristics”, Renew. Energy, 79, 14-19.
[https://doi.org/10.1016/j.renene.2014.08.041]

-
Choi, Y.S., Choi, S.K., and Jeong, Y.W., 2014, “Development of a tilted-slide reactor for the fast pyrolysis of biomass”, Environ. Prog. Sustain. Energy, 33(4), 1405-1410.
[https://doi.org/10.1002/ep.11888]

-
Vitázek, I., Šotnar, M., Hrehová, S., Darnadyová, K., and Mareček, J., 2021, “Isothermal kinetic analysis of the thermal decomposition of wood chips from an apple tree”, Processes, 9(2), 1-10.
[https://doi.org/10.3390/pr9020195]

-
Encinar, J.M., and González, J.F., 2008, “Pyrolysis of synthetic polymers and plastic wastes. Kinetic study”, Fuel Process. Technol., 89(7), 678-686.
[https://doi.org/10.1016/j.fuproc.2007.12.011]

-
Ceamanos, J., Mastral, J.F., Millera, A., and Aldea, M.E., 2002, “Kinetics of pyrolysis of high density polyethylene. Comparison of isothermal and dynamic experiments”, J. Anal. Appl. Pyrolysis, 65(2), 93-110.
[https://doi.org/10.1016/S0165-2370(01)00183-8]

-
Westerhout, R.W.J., Waanders, J., Kuipers, J.A.M., and Van Swaaij, W.P.M., 1997, “Kinetics of the low-temperature pyrolysis of polyethene, polypropene, and polystyrene modeling, experimental determination, and comparison with literature models and data”, Ind. Eng. Chem. Res., 36(6), 1955-1964.
[https://doi.org/10.1021/ie960501m]

-
Sawaguch, T., Inami, T., Kuroki, T., and Ikemura, T., 1980, “Studies on thermal degradation of synthetic polymers. 12. Kinetic approach to intensity function concerning pyrolysis condition for polyethylene low polymer”, Ind. Eng. Chem. Process Des. Dev., 19(1), 174-179 .
[https://doi.org/10.1021/i260073a030]

-
Sogancioglu, M., Yel, E., and Ahmetli, G., 2017, “Pyrolysis of waste high density polyethylene (HDPE) and low density polyethylene (LDPE) plastics and production of epoxy composites with their pyrolysis chars”, J. Clean. Prod., 165, 369-381.
[https://doi.org/10.1016/j.jclepro.2017.07.157]

-
Das, P., and Tiwari, P., 2017, “Thermal degradation kinetics of plastics and model selection”, Thermochim. Acta, 654, 191-202.
[https://doi.org/10.1016/j.tca.2017.06.001]

-
Aguado, J., Sotelo, J.L., Serrano, D.P., Calles, J.A., and Escola, J.M., 1997, “Catalytic conversion of polyolefins into liquid fuels over MCM-41: Comparison with ZSM-5 and amorphous SiO2 - Al2O3”, Energy Fuels, 11(6), 1225-1230.
[https://doi.org/10.1021/ef970055v]

-
Wang, G., Li, W., Li, B., and Chen, H., 2008, “TG study on pyrolysis of biomass and its three components under syngas”, Fuel, 87(4-5), 552-558 .
[https://doi.org/10.1016/j.fuel.2007.02.032]

-
Yang, H., Yan, R., Chen, H., Zheng, C., Lee, D.H., and Liang, D.T., 2006, “In-depth investigation of biomass pyrolysis based on three major components: Hemicellulose, cellulose and lignin”, Energy Fuels, 20(1), 388-393.
[https://doi.org/10.1021/ef0580117]