탄화수소계 전해질막 기반 막-전극접합체 제조를 위한 전사 기술
© 2017 by the The Korean Society for New and Renewable Energy
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
This study investigated the effects of the proton-exchanging conditions of the sulfonated poly (ether ether ketone) (sPEEK) membranes on the decal transfer rate. Various pre-treatment conditions of proton-exchanging the sPEEK membranes were used in terms of the acid concentration, temperature and time. The sPEEK membranes were analyzed to examine the effects of the acid concentration, temperature, and immersion time. The proton conductivities of the membranes were evaluated. The membrane electrode assembly, (MEA) of sPEEK membranes were fabricated by the decal transfer method. As a result, the pre-treated sPEEK membranes showed the highest proton conductivity (0.044 S cm-1, 0.16 meq g-1) immersed in 0.5 M H2SO4 for 2h, and it brought about the highest cell performance (0.39 A cm-2 @ 0.6 V, 0.269 W cm-2) due to a decrease in Ohmic resistance. Among the conditions for pre-treatment, the concentration of the pre-treatment acid solutions was found to be the most significant factor determining the proton conductivity of the membranes.
Keywords:
Fuel cell, proton exchange membrane, sPEEK composite membrane, proton conductivity, decal method키워드:
연료전지, 수소 이온 교환막, 술폰화 폴리에테르에테르케톤 복합막, 수소 이온전도도, 전사 방법1. 서 론
수소 이온 교환막 연료전지(PEMFC, proton exchange membrane fuel cell)는 높은 전류밀도와 소음이 적으며, 환경오염 물질이 발생시키지 않는 장점으로 많은 연구가 진행되고 있다. 연료전지는 수소와 산소의 에너지를 고분자 전해질막을 이용하여 화학반응에 의해 전기에너지와 열에너지로 변화 가능하며, 부산물로는 발생되는 간단하면서도 높은 효율의 친환경적인 신재생 에너지 기술이다.[1,9]
PEMFC에서 성능과 내구성을 결정짓는 막-전극 접합체(Membrane electrode assembly, MEA)는 고분자 전해질막(Polymer electrolyte membrane)과 전극(Anode, Cathode)로 구성되어 있다. 이중 PEM은 PEMFC의 핵심 부품으로 현재 가장 대표적으로 활용되는 전해질막은 듀퐁사에서 제조한 NafionⓇ 막과 Solvey사의 AquivionⓇ 막이다. 하지만, 100도 이상의 고온, 50%이하의 낮은 가습조건에서는 기계적, 열적 안정성과 수소이온전도도 등의 물성이 급격히 감소하여 연료전지의 심각한 성능저하를 초래한다. 이러한 불소계 고분자 전해질막의 대안으로 생산단가가 저렴하고, 높은 열화학적 안정성 및 수소이온전도성을 갖는 술폰화 된 poly(ether ether ketone)(sPEEK), 술폰화 poly (arylene ether sulfone)(sPAES), polybenzimidazole (PBI)같은 탄화수소계 전해질막이 연구되고 있다.[10,12]
상용화를 위해 높은 40,000시간이상의 수명이 요구되고 있으나 낮은 온도 조건에도 전해질막의 낮은 내구성 및 열화에 의해 목표 수명을 달성하지 못하고 있다. 실제 전해질막의 열화는 운전 도중 전해질막이 얇아지거나 뚫려 양쪽 전극이 전기로 연결되 shorting 현상을 야기하여 MEA수명등을 저하시키게 되며, 이 현상들은 불소계 고분자 및 탄화수소계 막 모두에 적용된다. 보고된 연구 결과에 의하면, 전해질막의 열화는 열에 의한 열화(thermal defradation), 수축과 팽창에 의한 물리적인 열화(mechanical degradation)와 PEFC의 공기극에서 발생 되는 과산화수소와 하이드록시 라디칼이 전해질막 사슬의 말단 또는 술폰산그룹을 공격하는 화학적인 열화(chemical degradarion)등이 주요 열화의 원인이다. 또 다른 문제는 MEA 제법에 따른 전극열화이다. 전극 열화의 원인은 Pt의 용해, 응집, 이동, 금속착페 및 금속산화물 형성을 통한 촉매 활성면적의 감소로 보고되고 있다.[10,13]
이에 전해질막과 전극의 열화를 감소시키기위해 본 연구에서는 폴리이미드로 강화시킨 sPEEK 강화복합막을 이용하여, MEA 제조 방식들인 스프레이, 스퍼터링, 스크린 프린팅, 전착, 전사(decal) 방법들 중 전사방식을 이용하여 MEA를 제조하여 평가하였다.[14,15] sPEEK 강화복합막은 이온전도성 이오노머에 다공성 지지체가 지지하는 방식으로 기존 이오노머 막에 비해 기계적 내구성은 우수한 장점이 있다. 하지만 강화막이 건조와 함수 과정을 반복적으로 일어나게 되면 막 표면의 크랙 또는 강화막 내부의 캐비티가 형성될 수 있다. 이는 크랙을 통해 강화막 내부로 라디칼 확산에 의한 화학적 분해 가속 또는 캐비티에 의한 해당 부분의 막 눌림 현상이 일어 날 수 있다.[16,17] 이를 해결하기 위해 강화막과 전극의 접착 호환성을 극대화하여 전기저항을 최소화하기 위해 전사방식을 이용하여 MEA를 제조하였다. 하지만 이오노머막들과 다르게 강화복합막의 경우 표면이 단단하여 전사시 전사율이 낮아지게 되는 현상들이 발견되었다. 이를 해결하고 최적의 전사율을 보이는 전사방식을 sPEEK 강화복합막의 황산에서의 다양한 전처리를 통해 최적화하였다.
본 연구에서는 sPEEK 강화복합막을 열, 시간, 황산의 농도등의 조건을 달리하여 변화된 강화복합막의 물성을 평가하였다. 또한, 전사방식을 이용하여 MEA를 제조하여 이의 전기화학적 분석을 진행하였다.
2. 실험 및 방법
2.1 sPEEK 강화막의 전처리 과정
술폰화된 PEEK 막은 ㈜코오롱 중앙연구원으로부터 제공받았다. sPEEK 막은 폴리이미드로 강화시킨 것으로 30㎛막을 사용하였다. sPEEK 막을 Na+폼에서 H+폼으로 치환하기 위해 0.5, 1, 2M의 황산 용액(95wt% H2SO4, Junsei)을 이용하여, 대기압, 80°C 항온조 하에 2시간 동안 전처리 후, 상부교반 중인 증류수에서 80°C 항온조 하에 2시간 동안 세척을 진행하고, 80°C 오븐에서 12시간 건조시켰다(Fig. 1).
2.2 막-전극 접합체(MEA) 제조
촉매 슬러리를 제조하기 위해 40wt% Pt/C촉매(Johnson-Matthey), isoprophyl alchhol(IPA, Junsei), 5wt% Nafion ionomer solution(D521, EW=970~1052g/eq, Dupont)을 넣고 교반을 한다. 제조된 촉매 슬러리의 조성은 Table 1에 정리하였다. 교반 방법은 마그네틱 교반기로 10분 교반 후 초음파 세척기로 1시간 교반 후 다시 마그네틱 교반기로 overnight 교반한다. 그 후 막-전극 접합체를 만들기 전에 30분 정도 초음파 세척기로 교반 한다. 제조된 촉매 슬러리 도포는 닥터 블레이드 방식으로 이형 필름인 Kapton 필름(Dupont, USA) 상에 슬러리를 박막코팅하여 실온에서 12시간 이상 건조하였다.
두께가 30㎛인 sPEEK 강화 복합막을 이용하여 막 양면에 데칼방법에 의해 Pt/C 전극입자를 130 bar, 135°C, 8분동안 처리 하여 전사하였다. Anode와 cathode 모두 Pt 함량이 0.4mg cm-2인 MEA를 제조하였다. 또한 기체확산층(Gas diffusion layer, GDL)은 SGL사의 10BC 제품을 사용하였다.
2.3 술폰화 된 PEEK 강화막의 특성 분석
sPEEK 강화막의 이온전도도는 임피던스 스펙트로스코피(SP-150, Bio-Logic Science Instruments, France)를 사용하여, 전극 시스템에서 0.1~105Hz의 주파수 범위, 5mV의 전압세기를 가지는 교류전원에서 측정하였다. 이렇게 구한 고분자전해질 막의 impedance R값을 아래의 식을 이용해 수소 이온전도도 σ값을 구하였다.
| (1) |
여기서, σ는 수소 이온전도도, L은 전압 측정을 위한 전극 사이의 거리, R은 고분자 전해질 막의 impedance, W는 막의 너비, 그리고 D는 막의 두께이다.
함수율(Water uptake, WU)은 샘플막의 젖은 무게와 건조 무게의 차이를 측정하여 결정하였으며, 이온교환용량(Ion-exchange capacity, IEC)은 산-염기적정을 통해 측정하였다. 전해질막 샘플을 12 시간 동안 상온에서 1M의 NaCl 용액에 담지 한 후 이 용액을 0.01N의 수산화나트륨 용액으로 848 Titrino plus을 이용하여 적정하여 IEC값을 구하였다.[18,20]
2.4 sPEEK MEA의 성능 및 전기화학적 특성 분석
MEA의 성능 및 특성은 I-V 분극곡선, 전기화학적 표면적(Electrochemical surface, ECSA), impedance 분석(High frequency resistance, HFR) 및 수소투과전류밀도(Hydrogen crossover current density, HCCD)등을 측정하여 비교하였다. 각각의 분석시 전극면적이 9cm2인 셀과 station(CNL Energy Co.)를 사용하였으며, 셀의 체결압은 60kg f를 사용하였다. 다양한 MEA의 성능 분석시의 station 조건은 Table 2에 나타내었다.
I-V 분극곡선은 anode와 cathode에 수소와 공기를 공급(화학양론비 H2:Air=1.5:2)하고, Loader를 이용하여 전류 변화에 따른 전압을 측정하였다.
임피던스(@0.6V, 0.1~105Hz의 주파수 범위, 5mV의 전압세기를 가지는 교류전원), ECSA(Scan rate 30mV s-1)및 HCCD(Scan rate 1mV s-1)는 potentiostat(SP-150, Bio-Logic Science Instruments, France)를 사용하여 측정하였다.[21,22]
3. 결과 및 고찰
본 연구에서는 sPEEK 강화복합막을 이용하여 전사방식을 통해 최적의 MEA제조를 위해 각기 다른 농도의 황산, 열, 시간의 전처리과정을 통해 막의 물성을 평가였다. Fig. 2의 사진을 보게 되면 황산에서 전 처리 후 막의 색이 투명한 색에서 노란색을 띄는 막으로 변한 것을 확인 할 수 있었다.
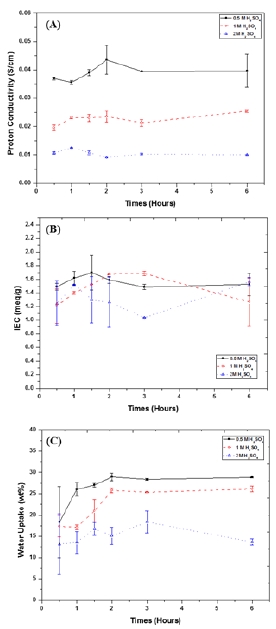
전처리 시 sPEEK 막의 술폰화 비율이 변화가 일어날 수 있다고 판단이 되었고, 전처리를 통해 변화된 막의 물성을 변화를 확인하기 위해 수소 이온전도도, IEC 및 함수율을 측정하였다. sPEEK막은 술폰화 비율에 따라 이온전도도 및 IEC등의 중요한 특성에 영향을 미치게 되다고 보고되었다.[20] 실제 각기 다른 농도의 85°C 황산에서 시간별로 전처리를 한 후 물성평가를 진행하였고, Fig. 3에 그 결과를 나타내었다. 결과 처리한 황산의 농도에 따라 각기 다른 수소 이온전도도, IEC 및 함수율을 보였으나, 처리 시간에 따른 영향은 크게 보이지 않았다. 0.5M의 85°C 황산용액에서 처리한 sPEEK 강화복합막이 가장 높은 수소 이온전도도인 0.044S cm-1및 IEC인 0.16meq g-1을 보였으며, 이는 2M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 이온전도도 보다 약 80% 증가한 값이다. 또한 함수율은 약 1.5배 높은 결과 값을 보였으며, 전처리 2시간 후의 결과를 Table 3에 나타내었다.
연료전지 전극 내에서 연료가스의 확산 및 촉매 접촉이 용이하게 형성되기 위해 전극 촉매 표면에 반응가스의 흡착이 원활하게 이루어져야 한다.[24] 이를 위해 촉매 슬러리 제조 시 이오노머 함량을 30%로 고정하였으며, 40wt% Pt/C를 사용하여 제조한 후 분산을 위해 초음파 세척 및 교반을 같이 이용하였다. 제조된 촉매슬러리를 이용하여 이형 필름 위에 코팅하였고, 크랙이 없는 형태로 건조하기 위해 실온에서 건조하였다. 다양한 조건의 전처리 된 sPEEK 강화복합막을 이용하여 전사 방법 통해 MEA를 제조하였다. 전사된 후의 이형필름 및 MEA의 사진을 Fig. 4에 보여주었고, 실제 전사율을 Table 4에 나타내었다. 전사 조건은 130 bar, 135°C, 8분동안 처리 하여 전사하였다. 본 연구에 사용된 전사 조건은 본 연구팀의 선행연구를 통하여 sPEEK 강화복합막의 전사조건을 최적화한 것이다. 실제 낮은 온도 또는 높은 온도에서는 전사율이 70%가 넘지 않았으며, 압력 및 시간에 따른 전사율 변화도 확인하였다. Table 4에서 보여준 전사율을 확인 하게 되면 전처리의 영향에 따른 전사율에는 높지 않음을 확인하였고, 모든 전사율은 93%이상의 높은 전사율을 보였다.
제조된 MEA들 중 각 각기 다른 농도의 황산 전처리 중 2시간처리한 sPEEK 강화복합막을 이용하여, MEA 테스트를 통해 분석을 하였다. MEA 테스트의 조건은 70°C, 상대가습 100%의 조건에서 평가되었다.
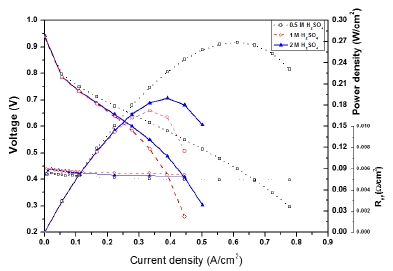
Fig. 5에 I-V 분극 곡선, Fig. 6에 임피던스 분석을 나타내었으며, 모든 단위 전지에서의 열림회로 전위(OCV, open circuit voltage)는 0.94V로 유사함을 보였다. 전류밀도가 낮은 0.5A cm-2이하의 저전류 밀도에서는 sPEEK 강화복합막의 전처리와는 무관하게 성능이 거의 유사하였고, 전류밀도가 증가함에 따라 앞의 수소 이온전도도의 결과와 같이 0.5M의 85°C 황산용액에서 처리한 sPEEK 강화복합막이 가장 높은 전류 밀도인 0.6V에서 0.39A cm-2와 최대출력밀도인 0.269W cm-2를 나타내었다. 하지만 수소이온전도도의 결과와 상이하게 2M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 MEA의 성능이 1M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 MEA 보다 높게 나온 것을 확인 할 수 있었다. 하지만 성능의 차이는 0.5M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 MEA의 성능차이보다 낮은 것을 확인 할 수 있었으며, 영향을 미친 요인으로 I-V 곡선의 기울기를 보면 막의 저항의 차이가 있음을 확인 할 수 있었으며, HFR값의 차이로도 확인이 가능하다. 동일한 막인 sPEEK의 전처리를 통해 막의 물성 변화가 생기며, 이를 통해 MEA의 성능까지 영향을 보인 것으로 판단이 된다.
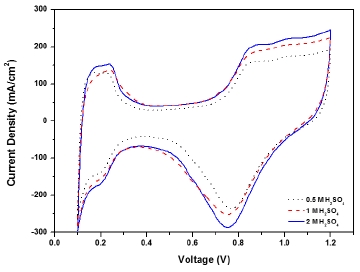
Fig. 7에서는 MEA 성능에 미치는 전극의 활성면적(ECSA)를 나타내었으며, Table 5에서는 MEA성능 분석을 정의하였다. ECSA의 가장 높은 MEA와 낮은 MEA의 차이는 20%내외로 약 3m2 Pt/gPt이 나며, 2M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 전극의 활성면적이 0.5M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 MEA 보다 높게 나온 것을 확인 할 수 있었으나, 0.5M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 MEA의 I-V 성능은 높아 전극의 영향은 작음을 확인하였다.
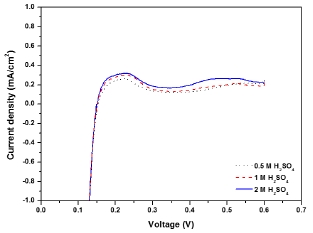
Fig. 8은 MEA OCV 및 성능에 미치는 전해질 막의 투과도 영향을 파악하기 위해 수소투과도를 LSV로 측정하였다. 탄화수소막의 일반적인 특징으로 가스 투과도가 낮은 것이 특징이나. 얇은 형태의 강화복합막의 경우 막의 저항을 줄일 수 있으나 가스 투과도가 증가할 수 있다. PEMFC에서는 막의 열화는 주로 라디칼에 의해서 발생되고, 발생된 라디칼은 수소와 산소가 막을 투과해 전극 상에서 반응해 발생되므로 가스 투과도가 감소하게 되면 내구성 및 열화 안정성이 높아진다. 본 MEA에서의 수소투과도는 0.4V기준 0.12~0.19mA cm-2로 막 수소투과도가 낮아 가스 투과에 의한 OCV 변화가 크지 않음을 확인하였다.
4. 결 론
본 연구에서는 sPEEK 강화복합막을 열, 시간, 황산의 농도 등의 조건을 달리하여 변화된 강화복합막의 물성을 평가하였다. 또한, 전사 방식을 이용하여 MEA를 제조하여 이의 전기화학적 분석을 진행하였다. 전처리를 통해 변화된 막의 물성을 변화를 확인하기 위해 수소 이온전도도, IEC 및 함수율을 측정하였다. 0.5M의 85°C 황산용액에서 처리한 sPEEK 강화복합막이 가장 높은 수소 이온전도도인 0.044S cm-1및 IEC인 0.16meq g-1을 보였으며, 이는 2M의 85°C 황산용액에서 처리한 sPEEK 강화복합막의 이온전도도 보다 약 80% 증가한 값이다. MEA의 성능 및 특성은 I-V 분극곡선, 전기화학적 표면적(Electrochemical surface area, ECSA), 임피던스 분석(High frequency resistance, HFR) 및 수소투과전류밀도(Hydrogen crossover current density, HCCD)등을 측정하여 비교하였다. 0.5M의 85°C 황산용액에서 처리한 sPEEK 강화복합막이 가장 높은 전류 밀도인 0.6V에서 0.39A cm-2와 최대출력밀도인 0.269W cm-2를 나타내었다.
Acknowledgments
본 연구는 2015년도 산업통상자원부의 재원으로 한국에너지기술평가원(KETEP)의 지원(No.201 53030031720 및 No.20153010031920)을 받아 수행한 연구과제입니다.
References
- Kraytsberg, A., Yair, E. E., (2014), “Review of advanced materials for proton exchange membrane fuel cells”, Energy. Fuel, 28(12), p7303-7330.
-
Bakangura, E., Wu, L., Ge, L., Yang, Z., Xu, T., (2016), “Mixed matrix proton exchange membranes for fuel cells: State of the art and perspectives”, Prog. Polym. Sci, 57, p103-152.
[https://doi.org/10.1016/j.progpolymsci.2015.11.004]

-
Zhang, H., Shen, P. K., (2012), “Recent development of polymer electrolyte membranes for fuel cells”, Chem. Rev, 112(5), p2780-2832.
[https://doi.org/10.1021/cr200035s]

-
Peighambardoust, S. J., Rowshanzamir, S., Amjadi, M., (2010), “Review of the proton exchange membranes for fuel cell applications”, Int. J. Hydrogen. Energ, 35(17), p9349-9384.
[https://doi.org/10.1016/j.ijhydene.2010.05.017]

-
Sopian, K., Wan Daud, W. R., (2006), “Challenges and future developments in proton exchange membrane fuel cells”, Renew. Energ, 31(5), p719-727.
[https://doi.org/10.1016/j.renene.2005.09.003]

-
Shin, M.-S., Kang, M.-S., Park, J.-S., (2014), “Development of anion-conducting ionomer binder solutions for electrodes of solid alkaline fuel Cells”, J. Nanosci. Nanotechno, 14(10), p7793-7797.
[https://doi.org/10.1166/jnn.2014.9462]

-
Lee, W.-Y., Kim, M., Sohn, Y.-J., Kim, S.-G., (2016), “Analysis of a high temperature polymer electrolyte fuel cell combined with an organic Rankine cycle system”, New Renew. Energy, 12(2), p30-39.
[https://doi.org/10.7849/ksnre.2016.06.12.2.30]

-
Lee, W.-Y., Kim, M., Sohn, Y.-J., Kim, S.-G., (2017), “Analysis of a high temperature polymer electrolyte fuel cell based trigeneration system”, New Renew. Energy, 13(2), p59-68.
[https://doi.org/10.7849/ksnre.2017.6.13.2.059]

-
Kim, E., Yim, S., Bae, B., Yang, T., Park, S., Choi, H., (2015), “Self-humidifying electrodes at low humidity for polymer electrolyte membrane fuel cells (PEMFCs)”, New Renew. Energy, 11(4), p46-51.
[https://doi.org/10.7849/ksnre.2015.12.11.4.46]

-
Lee, H. J., Choi, Y.-W., Yang, T.-H., Bae, B. C., (2014), “Hydrocarbon composite membranes with improved oxidative stability for PEMFC”, J. Korean Electrochem. Soc, 17(1), p44-48.
[https://doi.org/10.5229/jkes.2014.17.1.44]

-
Yuk, J. O., Lee, S. J., Yang, T.-H., Bae, B. C., (2015), “Synthesis and characterization of multi-block sulfonated poly(arylene ether sulfone) polymer membrane with different hydrophilic moieties for PEMFC”, J. Korean Electrochem. Soc, 18(2), p75-80.
[https://doi.org/10.5229/jkes.2015.18.2.75]

-
Lee, S. Y., Kim, H. J., Nam, S. Y., Park, C. H., (2016), “Synthetic strategies for high performance hydrocarbon polymer electrolyte membranes (PEMs) for fuel cells”, J. Membr. Sci, 26(1), p1-13.
[https://doi.org/10.14579/membrane_journal.2016.26.1.1]

-
Jeong, J.-J., Shin, Y.-C., Lee, M.-S., Lee, D.-H., Na, I.-C., Lee, H., Park, K.-P., (2013), “Characteristics of Poly (arylene ether sulfone) membrane for proton exchange membrane fuel cells”, Korean Chem. Eng. Res, 51(5), p556-560.
[https://doi.org/10.9713/kcer.2013.51.5.556]

-
Scofield, M. E., Liu, H., Wong, S.S., (2015), “A concise guide to sustainable PEMFCs: recent advances in improving both oxygen reduction catalysts and proton exchange membranes”, Chem. Soc. Rev, 44(16), p5836-5860.
[https://doi.org/10.1039/c5cs00302d]

-
Xu, W., Wu, Z., Tao, S., “Recent progress in electrocatalysts with mesoporous structures for application in polymer electrolyte membrane fuel cells”, J. Mater. Chem. A, 4(42), p16272-16285.
[https://doi.org/10.1039/c6ta05304a]

-
Kim, D.-H., Park, J.-H., Seo, S.-J., Park, J.-S., Jung, S., Kang, Y. S., Choi, J.-H., Kang, M.-S., (2013), “Development of thin anion-exchange pore-filled membranes for high diffusion dialysis performance”, J. Membr. Sci, 447, p80-86.
[https://doi.org/10.1016/j.memsci.2013.07.017]

- Zhang, B., Zhuang, X.P., Cheng, B., Wang, N., Ni, Y., (2014), “Carbonaceous nanofiber-supported sulfonated poly (ether ether ketone) membranes for fuel cell applications”, Mater. Lett, 11, p248-256.
-
Park, J.-S., Shin, M.-S., Sekhon, S.S., Choi, Y.-W., Yang, T.-H., “Effect of annealing of nafion recast membranes containing ionic liquids”, J. Korean Electrochem. Soc, 14(1), p9-15.
[https://doi.org/10.5229/jkes.2011.14.1.009]

-
Lee, H. J., Choi, Y.-W., Yang, T.-H., Bae, B. C., “Hydrocarbon composite membranes with improved oxidative stability for PEMFC”, J. Korean Electrochem. Soc, 17(1), p44-48.
[https://doi.org/10.5229/jkes.2014.17.1.44]

-
Shin, M.-S., Oh, G.-H., Park, J.-S., “Preparation and characterizations of ferroxane-Nafion composite membranes for PEMFC”, Membr. J, 26(2), p135-140.
[https://doi.org/10.14579/membrane_journal.2016.26.2.135]

-
Shin, M.-S., Byun, Y.-J., Choi, Y.-W., Kang, M.-S., Park, J.-S., (2014), “On-site crosslinked quaternized poly (vinyl alcohol) as ionomer binder for solid alkaline fuel cells”, Int. J. Hydrogen. Energ, 39(29), p16556-16561.
[https://doi.org/10.1016/j.ijhydene.2014.03.181]

- Sambandam, S. K., Ramani, V., (2007), “Effect of IEC and loading of cathode SPEEK binder on kinetic and transport properties of all-SPEEK MEAs”, ECS Trans, 11(1), p105-116.
- Song, J.-M., Woo, H.-S., Sohn, J.-Y., Shin, J., “12HPW/meso-SiO2 nano composite CSPEEK membranes for proton exchange membrane fuel cells”, J. Ind. Eng. Chem, 36, p132-138.
- Lee, H.R., Lee, S.-H., Hwang, B.-C., Na, I.-C., Lee, J.-H., Oh, S.-J., Park, K.-P., “Study on degradation of MEA using sulfonated poly(ether ether ketone) membrane in proton exchange membrane fuel cells”, Korean Chem. Eng. Res, 54(3), p305-309.