용융탄산염 연료전지용 탈황 흡착제 적용을 위한 거창 화강석 석분 슬러지의 유리화 과정 및 유리화 특성 분석
Copyright © 2016 by the New & Renewable Energy
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
The vitrification processes and characteristics of Geochang granite stone sludge were investigated for the application of desulfurization sorbent of Molten Carbonate Fuel Cell (MCFC). From the X-ray fluorescence analysis (XRF) results using Geochang granite stone sludge, it was confirmed that the network formers (SiO2 and Al2O3) in granite stone sludge were present between 83.2 and 87.2wt% and the rest was comprised of network modifiers (K2O, Na2O, CaO, Fe2O3 and MgO). When Borax (Na2B4O7-10H2O) was added in the granite stone sludge system for promoting the decomposition and reducing the melting viscosity of refractory SiO2 and Al2O3 comprising of stone sludge, it was observed that the melting point of the granite stone sludge system was reduced by more than 400°C and the optimized melting temperature for granite stone and borax systems was around 1400°C when comparing X-ray diffraction analysis (XRD) results. Phase transitions and thermal reactions of granite stone sludge systems were also investigated from thermal analysis using Thermogravimetric Analysis (TGA)/ Differential Scanning Calorimeter (DSC).
Keywords:
Molten carbonate fuel cell, Vitrification, Glass, Granite stone sludge, Borax키워드:
용융탄산염 연료전지, 유리화, 유리, 화강석 석분 슬러지, 보락스1. 서 론
석분 슬러지는 석산에서의 채석 과정 중 절단 공정과 석재 가공 공장에서의 석재의 절삭, 연삭 및 연마 공정 그리고 석재 조형물 가공중의 연삭 공정 중에 발생하여 입도가 매우 작은 미분 상태로 존재하게 된다. 이 부산물들은 건식가공 상태에서는 분말 상태로 존재하나, 습식가공 또는 부산물 처리 과정에서 사용되는 물과 침전제 등과 같은 액체와 혼합되면 겔 형상으로 존재하게 된다. 국내 3대 화강석 산지 중의 하나인 거창군 내에서 1일에 약 43톤 정도의 화강석 석분 슬러지가 발생하게 되는데, 이를 처리하기 위해서 거창군 내 석재 가공공장에서는 연간 약 3억 원의 비용을 지출하고 있다. 또 위탁업체의 처리용량이 제한되어 야적장에 쌓아둔 석분 슬러지가 빗물에 쓸려 인근 도로변에 유출되거나 불연성형태로 매립되어 환경오염의 문제가 되고 있다.[1] 이러한 문제점을 해결하기 위해 화강석과 같은 화산암의 일종인 현무암을 자원으로 이용할 수 있는 섬유 제조 공법은 이미 상업화가 진행되었을 정도로 오래 전부터 연구된 분야이다. 구체적으로는 현무암의 방사 공정은 1923년 구소련의 Paul 등에 의해 최초로 특허출원 되었으며 이후 구소련 정부의 지원 하에 다양한 연구가 개시되었다. 현무암과 유리의 섬유화 공정은 매우 유사하며, 원료를 용융시킨 후 공급관(토관)을 통해 방사구로 이동시키고 용융체를 유체역학적 압력으로 배출하는 과정을 통해 유리섬유를 얻게 된다.[2,3]
유리섬유의 물리적 특성과 안정성은 화학적 조성에 의해 영향을 받게 되는데, 이는 공정요소에 따라 달라질 수 있으며, 용융체의 점도 및 공정상의 온도 등에 크게 의존한다.[4-6] 예를 들어서 일반적으로 유리 제조 시 원료산화물을 망목구성산화물과 망목수식산화물로 구분할 수 있으며, 망목구성산화물의 경우 망목구조의 뼈대를 형성하는 역할을 하며, 망목수식산화물의 경우 망목구성산화물의 결합을 끊고 망목구조의 끝단에 결합하게 되어 비정질상의 안정화를 돕거나 녹는점을 낮추는 역할과 유리의 물리적 성질을 변화시키게 된다.[5] 또한 원료내부의 산화물의 조성에 따라 용융체의 점도를 예측할 수 있는데, 이산화규소(SiO2)와 산화알루미늄(Al2O3)은 용융체의 점도를 높이며, 기타 성분은 점도를 낮추는 역할을 하게 된다.[3,4,7,8]
본 연구에서는 이러한 높은 융점 및 용융점도 특성을 가지는 화강석 석분 슬러지를 이용하여 용융탄산염 연료전지(Molten Carbonate Fuel Cell, 이하 MCFC)에 적용될 탈황 흡착제의 지지체로 적용하기 위한 타당성 조사로서 화강석 석분 슬러지의 물성에 관한 특성을 연구하였다. 화강석 석분의 용융점과 용융점도에 변화를 주어 유리화 및 섬유화를 더욱 용이하게 하고자 융제로써 Na2B4O7-10H2O(이하 Borax)를 사용하였다. Borax는 저융점 망목구성산화물인 산화붕소(B2O3)와 유리제조의 대표적인 융제로써 알려져 있는 산화나트륨(Na2O)으로 이루어져 있어 1700°C의 SiO2융점을 1400°C 이하로 감소시키고 용융점도를 현저히 감소시킬 수 있다.[5,9,10]
화강석의 경우 현재 환경 폐기물로 취급 받고 있는 현실에서 화강석 석분 슬러지를 유리섬유로 적용하여 MCFC의 구동시 사용되는 디젤 연료의 탈황 흡착제로 제작하여 활용할 수 있다면, 석분 슬러지에 의한 환경오염문제를 해결하고, 경제적 비용절감 효과뿐만 아니라 MCFC에 의한 전력발생이 가능하므로 본 연구결과에서는 화강석 석분 슬러지에 Borax를 첨가하여 유리를 제조하는 방법을 소개하고 MCFC의 탈황 흡착제로 적용할 수 있는 거창 화강석 석분 슬러지의 유리화 과정 및 유리화 특성에 대해서 연구하였다.
2. 실험방법
2.1 석분 슬러지의 정량/정성 분석
실험에 사용한 거창 화강석 석분의 정량 / 정성적 분석을 위해 형광 X선 분석법(X-ray fluorescence analysis, 이하 XRF)과 X선 회절분석법(X-ray diffraction analysis, 이하 XRD)을 실시하였다. XRF 분석을 위한 전처리 과정으로는 거창 화강석 연구센터에서 제공된 분말상태의 화강석 석분 시료를 100°C의 건조기에서 6시간 건조 후 마노유발을 이용하여 분쇄하였다. 시료 전체에서의 균질한 성분비에 대한 신뢰성 확보를 위하여 3개의 독립된 500cc 용기에 담긴 시료를 6부분으로 나누어 분리한 후 각각 채취하여 Rigaku / RIX2100장비를 통해 분석하였다. XRD 분석 또한 건조된 분말상태의 화강석 석분 슬러지 시료를 마노유발을 사용해 분쇄하였고, Rigaku / SmartLab 장비를 이용하여 가속전압 45kV, 전류 200mA, 주사속도 1°/min및 주사범위 5-95°(=2Ɵ)의 조건으로 분석하였다.
2.2 화강석 석분의 유리화 실험
유리화 실험의 원료로써 분말상태의 거창화강석 석분 슬러지와 융제로써 Borax를 사용하였고, 현재 상업화가 진행 중인 현무암 섬유와의 비교를 위해 화강석 석분에 추가로 산화물을 첨가하는 방식으로 인위적으로 제작한 현무암조성을 이용하였다. 거창 화강석 석분 슬러지와 Borax, 인공적인 현무암 석분을 사용하여 8종의 시편을 제조하였으며 Table 1에 그 샘플명과 조성을 정리하였다. 유리화 실험 과정은 Fig. 1에 정리한 바와 같이 화강석 석분 및 Borax의 무게 칭량, 칭량 후 혼합, 알루미나 크로서블 담지, 전기로에 장입 후 1400°C에서 2시간 샘플 용융, 샘플 회수를 위한 금속 지지체 전처리, 용융된 샘플을 회수하여 금속 지지체에 주입 및 샘플 냉각으로 구성되는 7단계로 실시하였다.
2.3 열처리 온도에 따른 형상 변화, XRD 패턴 및 미세구조 분석
유리화 과정 중 시편의 온도구간별 시편의 형상변화와 XRD 패턴 변화를 비교 및 분석하기 위한목적으로 100°C의 온도간격으로 500-1400°C온도구간에서 1시간 동안의 열처리 후 형상변화 사진촬영과 함께 XRD분석을 실시하였다. Table 1의 GB10, GB11, BB10 및 BB11 4종의 조성에 대하여 실험하였으며 시편은 25mm × 6mm × 6mm 크기의 직사각형 금속 몰드를 이용하여 5MPa의 압력으로 일축 압축성형하여 시편을 제작하였다. 압축성형한 직사각형 펠렛을 직경 52mm의 알루미나 크로서블 덮개 중심부에 위치시킨 후 전기로에서 각각의 온도로 열처리를 실시하였으며 이 때 열처리 조건으로는, 분당 10°C의 속도로 승온하여 목표온도에서 1시간 유지하였다. 결정화를 방지하기 위해 열처리를 마친 시편은 전기로에서 꺼내어 공기 중에서 급랭하였다. 열처리 후 시편은 측면 및 상부에서 사진 촬영을 실시하였으며 마노유발에서 분쇄 후 분말형태의 시편을 이용하여 XRD분석을 실시하였다. 500-800°C에서 100°C간격으로 열처리한 GB11 시편을 가속전압 5-10kV, Spot Size 30, Working Distance 10-11mm의 조건에서 JEOL / JSM6390장비를 이용하여 미세구조 분석을 실시하였다.
2.4 열분석
Table 1에서 제시된 시편들의 열적 특성을 분석하기 위해 열 중량분석(Thermogravimetric Analysis, 이하 TGA)과 시차주사 열량측정법(Differential Scanning Calorimeter, 이하 DSC)을 이용하였다. Table 1의 GB10, GB11 및 BB11의 총 3개의 시편이 열분석에 사용되었다.
분석조건으로는 산화분위기에서 30-1450°C온도범위를 설정하여 분당 10°C의 속도로 승온과 감온 조건에서 측정하였으며 TGA 및 DSC 실험이 동시에 가능한 Setaram / Setasys16/18 장비를 사용하였다.
3. 결과 및 고찰
3.1 거창 화강석 석분 슬러지 시료의 정량/정성 분석결과
Fig. 2에서는 거창 화강석 석분 슬러지의 XRD 분석결과를 정리하였다. XRD결과의 8°,27°,28°에서 각각 Mica(K(Mg,Fe)2(AlSi3O10)(F,OH)2), Quartz(SiO2) 및 Albite (Na0.75Ca0.25)(Al1.26Si2.74O8)의 주 XRD 픽을 확인할 수 있으므로 거창 화강석 석분 슬러지는 Albite, Quartz 및 Mica의 광물로 구성된 것을 알 수 있다.
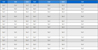
이러한 결과를 이용하여 거창 화강석 석분 슬러지의 산화물 질량 구성비와 구성성분 분석은 XRF결과를 통하여 실시하였으며 이를 Table 2에 정리하였다. 거창 화강석 석분 슬러지를 구성하고 있는 SiO2는 67.0-69.6wt%로 존재하였고 Al2O3는 16.1-17.6wt%의 범위에 존재하고 있다. K2O는 4.37-4.59wt%, Na2O는 2.92-3.62wt% 및 CaO는 2.21-3.54wt%의 범위로 존재하는 것을 확인하였다. 또한 Fe2O3는 2.20-2.27wt%, MgO는 0.539-0.650wt%, TiO2는 0.325-0.352wt%의 질량비 및 P2O5는 0.146-0.177wt%로 존재하였다.
유리 구성성분을 망목구성산화물(network forming-oxide)과 융제(fluxes),안정제산화물(stabilized-oxides) 및 착색제 / 유백제 / 청징제 역할을 하는 부산화물로 분류를 할 때, 거창 화강석 석분 슬러지의 경우 83.2-87.2wt%의 망목구성산화물과 나머지 부산화물로 구성되는 것을 확인하였다. 특히 SiO2및 Al2O3는 2000°C 이상의 고융점의 망목구성산화물로써 용융점도에 큰 영향을 미칠 것으로 판단할 수 있다.
3.2 석분 슬러지를 이용한 8종 시편의 유리화 분석
GB10, GB11, GB12, GB21, BB10, BB11, BB12 및 BB21시편 조성을 이용하여 1400°C의 온도에서 2시간 용융을 포함한 열처리 후 사진 촬영 결과는 Fig. 3(a)에 정리하였다. 높은 점도로 인해 알루미나 도가니에서 분리가 불가능했던 GB10 및 GB21 시편을 제외한 시편들은 유리화가 가능한 것을 알 수 있다. 이중 GB11시편의 XRD 패턴 변화를 Fig. 3(b)에 나타내었다.
열처리 전의 XRD 패턴은 거창화강석 석분과 Borax의 XRD 패턴이 혼합되어 있는 것을 알 수 있으며 1400°C의 온도에서 2시간 열처리 후 냉각 한 시편은 비정질 특유의 Broad한 XRD 패턴으로 상전이 한 것을 발견하였다. 즉 1400°C의 온도에서 2시간의 열처리 조건은 GB11 시편을 유리화 시킬 수 있는 온도 및 시간 조건으로 판단할 수 있다. 이러한 실험조건을 다른 시편에 적용시켰을 경우 GB10시편을 제외한 나머지 7종의 시편에서 모두 비정질 특유의 Broad한 XRD 패턴을 확인하였다. 또한 Borax의 첨가량 유무에 따라서 용융점도에 큰 차이가 발생한 것을 Fig. 3(a)에서 확인할 수 있다.
Borax를 화강석 분말 대비 동량 미만 또는 Borax를 혼합하지 않은 경우인 GB21, GB10시편의 경우에는 Fig. 3(a)에서 확인할 수 있듯이, 높은 점도에 의해서 시편제작에 사용된 알루미나 도가니에 강하게 결합되어 분리되지 않았다. 석분 슬러지와 같은 질량의 Borax첨가량을 보이는 GB21과 BB21를 비교하면, 더 낮은 용융점도에 의해서 BB21시편만 도가니에서의 분리가 가능하였다. 이는 점도의 차이로 판단할 수 있으며 구체적으로 화강석 조성에서의 높은 융점의 망목구성산화물(SiO2,Al2O3)에 비해, 현무암에서는 많은 양의 망목수식산화물이 존재하기 때문으로 판단된다. 이러한 점도의 차이는 추후 실험을 통해 data base화 할 것이다.

XRD patterns of (a) GB11 powder at room temperature and (b) GB11 after heat treatment at 1400°C for 2 hr
유리화 과정을 온도 별로 관찰하기 위해 진행한 XRD분석결과는 Fig. 4 및 5에서 정리하였다. GB10, BB10, GB11및 BB11 조성의 시편이 분석에 사용되었으며 열처리 온도에 따른 XRD 패턴의 비교분석을 위하여 500-1400°C온도구간에서 100°C간격으로 실시한 실험 데이터를 동일한 그래프에 나타내었다. Borax를 첨가하지 않은 시편 조성을 이용한 XRD분석 결과인 Fig. 4(a) 및 (b)에서 비교적으로 적게 포함된 광물인 Mica의 XRD 주 픽(2Ɵ = 8°)이 1200°C에서 완전히 소멸함을 확인할 수 있고, Quartz의 XRD 강도도 현저히 감소하는 것을 확인할 수 있다. Borax를 1:1의 질량비로 첨가해준 GB11, BB11시편의 경우 Fig. 5(a) 및 (b)의 XRD분석결과로부터 800°C에서 Mica XRD 주 픽의 소멸을 확인하였고, 동시에 Quartz의 XRD 주 픽의 상대적인 강도의 감소를 확인할 수 있다. GB11시편의 경우 1000°C에서 비정질상을 확인하였고, BB11의 경우에서는 900°C에서 비정질 특유의 Broad한 XRD 패턴을 확인 하였다. 따라서 Fig. 4와 5를 비교할 경우 융제로써 첨가한 Borax의 영향으로 석분 슬러지의 융점이 400°C 이상 감소되는 것을 알 수 있다.
Fig. 4 및 5의 모시편을 이용하여 실시한 측면 및 상부 사진촬영 결과를 Fig. 6에 정리하였다. Fig. 6(a)에서 정리한 GB10 조성의 시편은 1100°C까지는 형태의 변화는 없었으나 1000°C까지의 색상과 비교했을 때 상대적으로 붉은 계열의 색상을 보여주고 있다. 1200°C에서는 시편의 측면의 변화가 발생하였으며 1300°C에서는 용융이 활발하게 발생하여 최종생성물의 경우 droplet의 형태를 보이고 있었다. Fig. 6(b)에서 정리한 BB10의 경우 GB10과는 동일한 형상 변화를 보이고 있으나 droplet의 형태가 GB10에 비교했을 경우 100°C 낮은 온도인 1200°C에서 주로 발생하였다. Fig. 6(c) 및 (d)에서 측정한 Borax를 동일 질량 비율로 혼합한 GB11 및 BB11조성에서는 700°C에서 석분이 droplet 형태로 전이 된 것을 알 수 있다. 이것은 Fig. 4.및 5에서 제시된 XRD 결과와 동일한 결과로 판단 할 수 있다.

Photograph results of (a) GB10, (b) BB10, (c) GB11 and (d) BB11 after heat treatment in temperature ranges of 500-1400°C
Fig. 7은 GB10, GB11 및 BB11에 관한 승온 및 감온시의 열분석 결과를 나타내고 있다.
본 결과에서 검은색은 승온시의 TGA / DSC결과 나타내고 있으며 회색은 감온시의 TGA / DSC 결과를 제시하고 있다. GB10 시편의 열분석 결과인 Fig. 7(a)의 DSC 곡선에서는 200°C온도 이하에서의 흡열픽과 1200°C부근에서의 흡열픽을 확인 할 수 있다. 200°C 온도 이하에서의 흡열픽의 경우 석분 슬러지에 잔존하고 있는 수분이 제거되는 구간으로 판단 할 수 있으며 1200°C 부근에서의 흡열픽의 경우 석분 슬러지가 분해하여 용융이 시작되는 온도구간으로 판단 할 수 있다.
GB11 및 BB11시편의 열분석 결과인 Fig. 7(b) 및 (c)에서는 석분과 Borax의 화학반응에 관련된 특성을 확인할 수 있다. Fig. 7(a)에서 확인할 수 없는 450-500°C, 610-650°C 및 700-1200°C 구간의 흡열픽은 Borax 자체의 반응과 Borax와 석분 슬러지의 화학반응에 의한 열분해 특성이라는 것을 설명해준다. 또한 GB10시편에 비해 큰 폭의 무게감소를 통해 대부분의 무게감소가 Borax의 결정수 분해반응 및 Borax의 분해반응에 의한 것임을 알 수 있다. 요약하면 Fig. 7의 (a), (b) 및 (c)에서 정리된 결과에서 200°C 이하의 온도에서 확인할 수 있는 흡열픽은 석분 내에 흡수된 수분과 결정수의 증발에 의한 것으로 판단될 수 있고, 450-500°C 온도구간의 흡열픽을 Borax의 분해에 의한 특성으로 연계시킬 수 있다. 이는 Fig. 6의 500°C 시편에서 분해되어 비스킹화된 펠렛의 형상이 탈가스 작용에 의한 것임을 확인시켜준다. Fig. 6(c) 및 (d)에서 확인 할 수 있는 700°C 시편에서의 모서리연화현상을 610-650°C 부근의 흡열반응에 의한 것으로 판단할 수 있는데, 이는 Na2O와 B2O3로 분해된 Borax의 분해 및 용융에 의한 것으로 판단된다. 700-1000°C부근의 여러 번의 흡열반응을 Fig. 5의 Quartz, Albite 및 Mica의 상분해에 의한 XRD 픽의 강도 감소와 연계 시킬 수 있다.

TGA/DSC results of (a) GB10, (b) GB11 and (c) BB11 with increasing and decreasing temperature under air condition
XRD분석, 측면 및 형상변화 특성 및 TGA/DSC열분석실험을 통해서 거창 화강석 슬러지의 유리화 과정을 분석한 결과를 정리하면, 화강석 석분 슬러지 자체만으로는 1400°C 온도까지 열처리하였을 때 모유리 제작이 불가하였으며 석분 슬러지에 Borax를 첨가하였을 때 약 400°C의 융점 감소효과와 상당한 용융점도의 변화 효과를 얻을 수 있었고, 유리화를 위한 용융특성을 확보하기 위해서는 화강석 조성 대비 최소 동량이상의 Borax의 혼합이 필요한 것을 알 수 있다. 또한 화강석에 비해 현무암을 이용한 유리화가 약 100°C 가량 낮은 온도에서 유리화하였으며 이는 비교적 많은 망목수식체의 영향으로 판단할 수 있다.
3.3 SEM분석을 통한 미세구조 분석
Fig. 8에서 정리한 GB11시편의 500-800°C 온도조건에서의 표면 미세구조를 관찰한 결과를 통해 유리화 과정을 단계별로 분석하였다. Fig. 8(a)에서 확인할 수 있듯이 500°C 시편에서도 액상 소결 현상을 관찰할 수 있었지만, Quartz 및Albite등의 석분의 광물입자는 분말형태의 미세한 입자형태를 보인다. 따라서 석분에 의한 소결보다는 융점에 근접한 Borax에 의해 액상 소결이 진행됨을 알 수 있다. Fig. 8(b)의 미세구조 분석을 통해 600°C에서는 소결이 더욱 치밀하게 진행된 것을 알 수 있다. 석분 입자 주변에 기공 없이 Borax 성분에 둘러싸임을 확인할 수 있다. Fig. 8(c)의 경우 700°C의 열처리 구간에서는 Borax가 용융되어 표면의 굴곡이 사라짐을 확인할 수 있다. 또 평탄한 표면 위에 작은 돌기들을 관찰 할 수 있었는데, 석분 성분의 Borax 기지 내로의 용해에 의한 석분 성분의 편석의 흔적으로 판단된다. 마지막으로 Fig. 8(d)에서 확인할 수 있듯이 800°C에서는 석분 성분이 용융되면서 Borax 기지 내로 석분 성분이 용융되는 미세구조 특성을 확인하였다.
4. 결 론
본 연구에서는 화강석 석분 슬러지를 활용하여 MCFC의 탈황 흡착제의 지지체로 사용될 수 있는 모유리 제조 및 모유리의 유리화 과정에 대한 분석을 실시하였다.
실험에 사용된 거창 화강석 석분 슬러지의 XRD 및 XRF분석결과 Quartz, Albite 및 Mica의 광물로 이루어져 있으며, SiO2및 Al2O3의 고융점의 망목구성산화물(83.2-87.2wt%)과 나머지 망목수식산화물(K2O, Na2O, CaO, Fe2O3 및 MgO)로 구성되는 것을 확인하였다. 고융점의 SiO2 및 Al2O3의 분해를 촉진하고 용융점도에 변화를 주기 위해 Borax(Na2B4O7-10H2O)를 사용하였으며 열처리 온도별 형상관찰과 XRD 패턴 분석 실험결과의 비교를 통해 Borax에 의해 석분 슬러지의 용융점이 400°C 이상 감소함을 확인하였다. 1000°C의 열처리온도에서 완전한 비정질 상을 얻을 수 있었으며, 1400°C에서 용융이 가능한 온도조건을 확보하였다. 500-1400°C 구간에서 실시한 열처리 온도별 형상관찰 및 XRD패턴 분석과 TGA / DSC열분석 결과를 비교, 대응 시키는 과정을 통해 온도구간에 따른 상변화, 열역학적 반응을 확인할 수 있었다.
펠렛의 모서리 연화현상과 XRD 패턴을 통해 Borax를 첨가하지 않은 화강석 석분은 1200°C에서 유리화가 진행되고 현무암 석분은 1100°C에서 유리화가 진행됨을 알 수 있다. Borax를 동량 첨가한 석분의 경우 800°C에서 유리화가 진행되어 비정질의 Broad 한 XRD 패턴으로 변화하는 것을 확인할 수 있다.
Acknowledgments
본 연구는 2015년도 지식경제부의 재원으로 한국에너지기술평가원(KETEP)의 지원을 받아 수행한 연구 과제(300kW급 MCFC 디젤 연료전처리를 위한 탈황기 기반기술 개발)입니다. 이에 감사 드립니다.
References
-
Jung, S., Jeong, S., Chang, S., (2014), “Esitimation of ultimate methane and hydrogen sulfide yields for C&D waste and MSW using BMP test”, New & Renewable Ener, 10(1), p30-40.
[https://doi.org/10.7849/ksnre.2014.10.1.030]

-
Park, H.J., Park, S.M., Lee, J.W., Roh, G.C., Kim, J.K., (2010), “Studies of the melting characterization of basalt and its continuous fiber spinning”, Compo. Res, 23(3), p43-49.
[https://doi.org/10.7234/kscm.2010.23.3.043]

-
Sim, J., Park., C., Moon, D.Y., (2005), “Characteristics of basalt fiber as a strengthening material for concrete structure”, Composites: Part B, 36(6-7), p504-512.
[https://doi.org/10.1016/j.compositesb.2005.02.002]

-
Terry Lay, G. F., Rockwell, M.C., Wiltshire, J.C., Ketata, C., (2009), “Characteristics of silicate glasses derived from vitrification of manganese crust tailings”, Ceram. Int, 35(5), p1961-1967.
[https://doi.org/10.1016/j.ceramint.2008.10.035]

- 김병호, (2013), “유리공학”, 3rd ed, 청문각.
-
Kuo, Y.M., Huang, K.L., Wang, C.T., Wang, J.W., (2009), “Effect of Al2O3 mole fraction and cooling method on vitrification of an artificial hazardous material. Part 1: Variation of crystalline phases and slag structures”, J. Hazarad. Mater, 169(1-3), p626-634.
[https://doi.org/10.1016/j.jhazmat.2009.04.015]

-
Kim, Y., Oh, M.S., (2010), “Effect of cooling rate and alumina dissolution of the determination of temperature of critical viscosity of molten slag”, Fuel Process Technol, 91(8), p853-858.
[https://doi.org/10.1016/j.fuproc.2010.02.006]

-
Vassilev, S.V., Kitano, K., Takeda, S., Tsurue, T., (1995), “Influence of mineral and chemical composition of coal ashed on their fusibility”, Fuel Process. Technol, 45(1), p27-51.
[https://doi.org/10.1016/0378-3820(95)00032-3]

-
Wang .,, S, Zhang, C., Chen, J., (2014), “Utilization of coal fly ash for the production of galss-ceramics with unique performances: A Brief Review”, J. Mater. Sci. Technol, 30(12), p1208-1212.
[https://doi.org/10.1016/j.jmst.2014.10.005]

-
Jie, L.I., Mei-Fang, D.U., Bo, Y., Zhong-Xio, Z., (2008), “Quantum and experimental study on coal ash fusion with borax fluxing agent”, J. Fuel Chem. Technol, 36(5), p519-523.
[https://doi.org/10.1016/S1872-5813(08)60032-8]