구리박판의 열 산화법을 이용한 산화구리 나노선의 형성
© 2017 by the The Korean Society for New and Renewable Energy
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
The nanowire structure can be applied to a wide range of electronic and optical devices because of its electron confinement effect and high specific surface area. In particular, oxide-based nanowires can be applied to various fields including solar cells. Copper oxide has various phases and many advantages, such as low cost and no toxicity. In particular, cuprous oxide (Cu2O) can theoretically achieve a high conversion efficiency of ~20%. In this study, copper foil was annealed at various temperatures and copper oxide began to develop in the form of a nanowire at over 300°C. X-ray diffraction, scanning electron microscopy, and transmission electron microscopy confirmed that the nanowires grown at 400°C and 600°C crystallized in the stoichiometric Cu2O and CuO (cupric oxide) phases, respectively. This systematic work can contribute to the development of nanowire-based solar cells.
Keywords:
Nanowire, Copper oxide, Thermal oxidation, Cuprous oxide, Solar cell, Absorber layer키워드:
나노선, 산화구리, 열 산화, 제1산화구리, 태양전지, 흡수층1. 서 론
최근 한정된 화석에너지를 대체할 수 있는 신재생 에너지에 대한 관심이 점차 커져가고 있다. 신재생 에너지에는 태양전지나 태양열발전, 풍력발전, 조류발전, 지열발전 등이 있는데 그중 무한 청정 에너지원인 태양광발전에 대한 연구가 활발히 진행되어지고 있다.[1] 특히 친환경적이고 매장량이 풍부한 구리산화물 기반의 태양전지에 대한 관심도 커지고 있다. 구리 산화물은 다양한 상으로 존재할 수 있는데 그 중 Cu2O는 약 2.1 eV에 달하는 높은 밴드갭을 갖지만 태양전지에 적용되었을 때 이론적으로 약 20%에 달하는 효율을 낼 수 있다.[2,3] 또한 장기적으로 안정성을 갖고 무독성이라는 장점을 가지고 있으며 특히 풍부한 매장량과 낮은 가격 등의 장점을 가지고 있기 때문에 초저가형 태양광 발전에서 경쟁력 있는 물질이라 할 수 있다.[3-5] 쉬운 비교로 그동안 많은 연구가 이루어진 CdTe는 1 W 발전에 필요한 소재단가가 9.7E-02 cent/W이고 CIGS(CuInxGa(1-x)Se2)는 2.3E-02 cent/W이다.[6] 그에 비해 Cu2O는 3.6E-03 cent/W 정도로 CdTe나 CIGS에 비해 약 1/100에서 1/10수준의 발전 단가를 갖는다. 또한 약 4.9E-03 cent/W로 비슷한 발전 단가를 보이는 CZTS(Cu2ZnSnS4)의 경우 4원계 시스템으로 조성컨트롤이 어렵거나 2차상 형성 제어가 어렵다는 단점이 있다.[6-8]
이러한 장점들로 구리 산화물 기반의 태양전지는 최근 많은 관심을 받으며 연구가 진행되고 있다. 특히 가장 높은 효율을 보고한 일본의 T. Minami 그룹에서는 구리박판의 열 산화 방법을 통해 벌크 기반의 Cu2O 흡수층을 제작하였고 꾸준한 연구를 통해 최근 약 8.1%의 효율을 갖는 태양전지를 제작했다고 보고하였다.[9]
일반적으로 열 산화법을 이용한 구리 산화물 결정립의 합성은 800-1000°C의 산화 온도 구간에서 주로 이루어진다고 알려져 있다.[10] 그러나 Cu2O 결정립 성장 온도와 달리 나노선은 300-500°C에서 성장한다고 알려져 있고,[11,12] 우리는 다양한 온도에서 열 산화를 시도하여 각 조건에서 얻어진 구리 산화물에 대한 구조적 분석을 진행하였다. 특히 특정온도 이상에서 열처리를 진행하였을 때 나노선 구조를 얻을 수 있었는데 이에 대한 분석을 집중적으로 수행하였다.
나노선 구조는 전자 구속 효과와 높은 비표면적으로 인해 광・전자 소자에 폭넓은 응용이 가능하다.[13,14] 특히 산화물 기반의 나노선은 다양한 분야에 응용이 가능하기 때문에 큰 주목을 받고 있으며 많은 그룹에서 연구가 진행되고 있다.[13-15] 산화구리 나노선 구조는 열 산화 온도조절을 통해 Cu2O 나노선과 CuO 나노선을 선택적으로 제작이 가능할 것으로 예상되며 각각 다양한 분야에 적용이 될 수 있는데 대표적으로 CuO 나노선의 경우 센서나 p-type 전계 효과 트랜지스터 등의 분야에 적용될 수 있다.[14,16-19] 또한 이 연구에서 중점적으로 확인하고자 하는 Cu2O 나노선은 태양전지에 적용되었을 때 넓은 활성 영역을 갖기 때문에 더 많은 빛을 흡수할 수 있고 넓은 접합 영역과 높은 수집효율을 가질 수 있다. 또한 변형 완화 효과 및 전기적, 광학적으로 기존의 웨이퍼 기반 또는 박막 디바이스에 비해 더 향상된 특성을 가질 수 있다.[13,20-22] 우리는 본 실험을 통해 얻어진 결과가 추후 Cu2O기반 태양전지에 적용되었을 때 기존보다 특성 이 향상될 수 있을 것으로 기대하였다.
2. 실험 방법
우리는 순도 99.99%의 구리 박판을 대기압 공기분위기에서 전기로를 이용하여 열 산화를 시켜 각 공정조건에 따른 특성을 확인하였다. 두께 0.15mm, 12.5 × 12.5mm 크기의 구리 박판을 사용하였고 열처리 공정 전 암모니아수(Sigma Aldrich, NH4OH, ≥ 25%)와 증류수를 이용하여 각각 5분간 세척을 진행하였다. 전기로의 온도는 300°C, 400°C, 500°C, 600°C로 설정하였고 각각 2 시간 열처리 진행 후 전기로의 전원을 끄고 상온까지 냉각시켰다(Table 1).
산화 생성물은 X선 회절분석(X-ray diffraction, XRD, gonio scan, 20-80°), 주사 전자 현미경(field emission scanning electron microscopy, FE-SEM), 에너지 분산형 X선 분석(energy-dispersive X-ray spectroscopy, EDX), 투과 전자 현미경(transmission electron microscopy, TEM)측정 등을 통해 특성을 확인하였다.
3. 실험 결과 및 고찰
본 논문에서는 전기로를 이용하여 다양한 온도에서 구리 박판의 산화공정을 진행하였고 상의 변화와 나노선의 성장 및 형상에 대한 온도의 영향을 알아보기 위한 실험을 진행하였다.
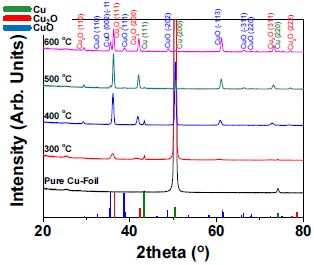
우리는 구리 박판을 300°C, 400°C, 500°C, 600°C에서 각각 2시간 동안 열처리를 진행하고 그에 따른 산화구리의 상변화를 XRD분석을 통해 알아보았다(Fig. 1). Fig. 1을 통해 순수한 구리 박판은 25.3°, 43.3°, 50.4°, 74.1° 부근에서 회절 피크(Cu, Cubic, JCPDS card #85-1326)가 나타나는 것을 확인할 수 있고 300°C 이상에서 열처리를 진행했을 때 Cu2O와 CuO상이 생기는 것을 관찰할 수 있다.
각 상의 온도에 따른 변화를 살펴보면 먼저 50.4° 부근의 Cu (200) 피크는 열처리 온도가 증가할수록 피크의 강도가 급격하게 감소하고 600°C에서 열처리를 진행했을 때 피크가 거의 사라진 것을 확인할 수 있다. 또한 43.3° 부근의 (111) 피크는 순수한 구리 박판과 400°C까지 열처리한 샘플에서 약한 강도의 피크가 보이나 500°C 이상에서 거의 사라지는 것을 볼 수 있다.
다음으로 Cu2O 회절 피크(Cu2O, Cubic, JCPDS card #78-2076)는 300°C부터 36.4°, 42.3° 부근에 (111)피크와 (200)피크가 생긴 것을 확인할 수 있으며 400°C이상부터 29.6°부근에 (110)피크와 78.5°부근에 (311)피크가 생긴 것을 볼 수 있다. 그리고 전체적으로 온도 증가에 따라 피크의 강도도 같이 증가하는 경향을 보임을 확인할 수 있다.
마지막으로 CuO 상(CuO, Monoclinic, JCPDS card #48-1548)은 300°C에서 열처리한 샘플에서 61.5° 부근에서 작은 피크가 생긴 것을 확인할 수 있고 열처리 온도 증가에 따라 피크의 수와 강도가 점점 증가하는 것을 볼 수 있다. 결론적으로 CuO 상은 대체적으로 Cu2O보다 고온에서 형성됨을 알 수 있으며 이는 온도가 높아질수록 구리와 산소의 반응이 더욱 활발해지고 이에 따라 구리상은 점점 줄어들고 CuO 상은 점점 증가하는 것으로 예측된다.
한편, XRD 분석은 구리 박판을 포함하여 그 위에 형성된 모든 결정화된 박막 및 나노선의 정보를 포함하기 때문에 먼저 형상을 확인하기 위해 SEM 분석을 진행하였다. Fig. 2는 각 조건별 SEM 이미지이다. 먼저, 기존의 구리 박판의 이미지와 비교했을 때 열처리 시 모든 온도 범위에서 표면에 구리 산화층으로 보이는 박막 형태가 관찰되었다. 또한, 400°C 이상 열처리 시 이러한 산화 구리층 위로 나노선들이 형성되었음을 확인할 수 있다. 특히 400°C에서 열처리를 진행한 샘플에서 형성된 나노선의 길이는 약 500-700nm정도로 관찰되다가 열처리 온도가 증가할수록 나노선의 길이가 최고 3-5㎛까지 성장하고 직경 또한 증가하는 것을 확인할 수 있다.
Fig. 3은 400°C 및 600°C에서 형성된 나노선의 고배율 SEM 이미지 및 EDX 분석 결과이다. 나노선의 성장기구(growth mechanism)는 두 가지가 있는데 VLS(vapor-liquid-solid)와 VS(vapor-solid)가 그것이다.[23,24] VLS 성장기구는 나노선의 성장을 위해 금속 촉매가 필요하며 나노선의 끝에 금속 촉매 입자가 관찰된다고 알려져 있다.[25,26] Fig. 3(a)와 (c)에서 나노선의 끝에 어떠한 금속 입자도 발견되지 않은 것을 확인할 수 있다. 또한 나노선의 직경은 금속 촉매입자의 크기에 의존하기 때문에 나노선의 성장에 직경변화가 없어야 하지만 Fig. 2에서 나노선의 직경이 열처리 온도에 따라 점점 두꺼워 지는 것으로 보아 VS 성장기구를 통해 성장한 것으로 추론하였다.
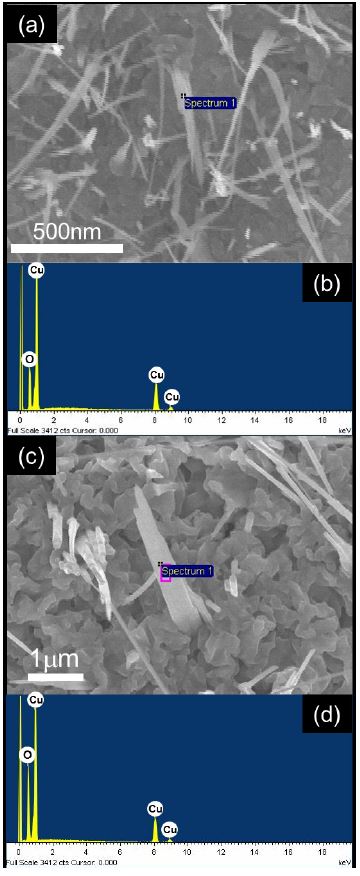
(a) 400°C 열처리를 진행한 샘플에서 형성된 나노선의 SEM 이미지 및 (b) EDX 측정 결과. (c) 600°C 열처리로 형성된 나노선의 SEM 이미지 및 (d) EDX 측정 결과
다음으로 Cu2O가 많이 형성된 400°C 열처리 샘플의 나노선과 CuO가 많이 형성된 600°C 열처리 샘플의 나노선의 성분 분석을 위해 SEM 기반의 point EDX측정을 진행하였다. 400°C 및 600°C 결과에 해당하는 Fig. 3(b)와 Fig. 3(d)를 비교했을 때 산소 비율이 차이를 보이는 것을 확인할 수 있다. 그리고 이 결과를 통해 구리와 산소의 비율을 정량화하면 400°C 열처리 조건에서 57:43으로 구리의 비율이 높은 것으로 나타났다. 또한, Fig. 3(d)의 600°C 열처리에서 구리와 산소의 비율은 42:58로 산소의 비율이 높은 것으로 나타났다. 그러나, 위에서 서술한 바와 같이 SEM-EDX 분석의 경우 기판 표면에 산화된 박막 층에 대한 정보를 포함하게 된다. 나노선 자체의 특성에 대한 보다 정확한 분석을 위해 초음파 세척기를 이용하여 산화구리 나노선만을 분리하여 TEM-grid에 올려 TEM 분석을 시행하였다.
Fig. 4는 400°C 및 600°C에서 열처리한 샘플 에서 얻어진 나노선의 TEM 결과이다. 먼저 두 조건에서 형성된 나노선의 직경을 비교해보면 400°C 및 600°C 나노선의 직경은 각각 약 39nm와 307nm로 측정되었다. 또한 Fig. 4(b) 및 (d)의 고해상도 이미지를 통해 결정립이 존재하지 않는 단결정 상태의 나노선이 형성되었음을 확인했다. 각 조건에서의 면간거리는 각각 2.46Å, 2.54Å으로 측정되었고 이는 Cu2O의 (111)면, 그리고 CuO의 (002)면에 해당한다.[27,28] 또한 원자간의 거리는 계속해서 일정한 것을 볼 수 있는데 이를 통해 다른 상이 섞이지 않고 단일상만 존재하는 것으로 판단하였다.

(a) 400°C 열처리를 진행한 샘플에서 형성된 나노선의 TEM 이미지 및 (b) 이를 확대한 이미지. (c) 600°C 열처리를 진행한 샘플에서 형성된 나노선의 TEM 이미지 및 (d) 이를 확대한 이미지
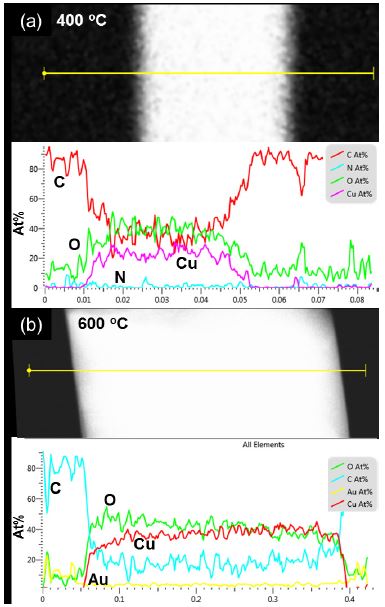
나노선 자체의 보다 정확한 성분 분석을 위해 line EDX측정을 진행하였다(Fig. 5). Cu와 O 이외에 N과 Au가 검출된 것을 확인할 수 있다. 이는 각각 암모니아수를 이용한 세척 및 TEM-grid 내 Au mesh에 의한 영향으로 판단된다. Fig. 5(a) 및 (b)를 통해 400°C 및 600°C 열처리로 형성된 나노선의 구리와 산소의 비율은 각각 약 2:1과 1:1임을 확인할 수 있다. 또한 나노선의 위치별로 EDX 분석 결과 길이 방향으로 모두 유사한 구리와 산소 비율을 지닌 것을 확인하였고 이는 나노선의 길이 방향에 대한 균일성을 의미한다. 따라서, 이러한 TEM 분석 결과로 미루어 보아 400°C 열처리로 형성된 나노선은 Cu2O, 600°C 열처리로 형성된 나노선은 CuO 상에 해당하는 것으로 판단하였다.
4. 결 론
구리박판의 간단한 열산화 공정 시 적절한 온도 제어를 통해 Cu2O 및 CuO 나노선을 형성할 수 있음을 확인하였다. XRD와 EDX 분석을 통해 열처리 온도가 증가함에 따라 구리 박판 표면에 산화층이 형성되고 400°C 이상 열처리 시 이러한 산화 구리층 위로 나노선이 형성됨을 확인할 수 있었다. TEM 및 EDX 분석을 통해 각각 400°C와 600°C 열처리 시 Cu2O와 CuO 나노선이 형성됨을 확인하였다. 추후 이러한 결과를 바탕으로 고효율 나노선 기반의 태양전지 개발이 기대된다.
Nomenclature
| Eg : | energy gap, eV |
| Tann. : | annealing temperature, °C |
subscript
| XRD : | X-ray diffraction |
| FE-SEM : | field emission scanning electron microscopy |
| TEM : | transmission electron microscopy |
| EDX : | energy-dispersive X-ray spectroscopy |
| VLS : | vapor-liquid-solid |
| VS : | vapor-solid |
Acknowledgments
본 연구는 미래창조과학부의 재원으로 한국연구재단(NRF-2015R1C1A1A02036616)과 산업통상자원부에서 시행한 지식경제 기술혁신사업의 에너지기술평가원(KETEP) 인력양성프로그램(20164030201310)에 의해 지원되어 작성되었습니다.
References
- Lee, D. H., Kim, Y. H., Song, J. D., Kim, S., (2009), “A Study on the Output Power Enhancement of GaAs/AlGaAs Solar Cell Using Concentration Method”, New. Renew. Ener, 5(3), p26-31.
-
Minami, T., Nishi, Y., Miyata, T., Nomoto, J. I., (2011), “High-efficiency oxide solar cells with ZnO/Cu2O heterojunction fabricated on thermally oxidized Cu2O sheets”, Appl. Phys. Express, 4(6), p062301.
[https://doi.org/10.1143/apex.4.062301]

-
Lee, S. W., Lee, Y. S., Heo, J., Siah, S. C., Chua, D., Brandt, R. E., Kim, S. B., Mailoa, J. P., Buonassisi, T., Gordon, R. G., (2014), “Improved Cu2O-based solar cells using atomic layer deposition to control the Cu oxidation state at the p-n junction”, Adv. Energy Mater, 4(11), p1301916.
[https://doi.org/10.1002/aenm.201301916]

-
Lee, Y. S., Heo, J., Siah, S. C., Mailoa, J. P., Brandt, R. E., Kim, S. B., Gordon, R. G., Buonassisi, T., (2013), “Ultrathin Amorphous Zinc-Tin-Oxide Buffer Layer for Enhancing Heterojunction Interface Quality in Metaloxide Solar Cells”, Energy Environ. Sci, 6(7), p2112-2118.
[https://doi.org/10.1039/c3ee24461j]

-
Minami, T., Nishi, Y., Miyata, T., (2015), “Heterojunction solar cell with 6% efficiency based on an n-type aluminum-gallium-oxide thin film and p-type sodiumdoped Cu2O sheet”, Appl. Phys. Express, 8(2), p22301.
[https://doi.org/10.7567/apex.8.022301]

- Group, R., Division, S., Berkeley, L., (2009), “Materials Availability Expands the Opportunity for Large-Scale Photovoltaics Deployment”, Environ. Sci. Technol, 43(6), p2072-2077.
- Mendis, B. G., Goodman, M. C. J., Major, J. D., Taylor, A. A., Durose, K., Halliday, D. P., (2012), “The role of secondary phase precipitation on grain boundary electrical activity in Cu2ZnSnS4 (CZTS) photovoltaic absorber layer material”, J. Appl. Phys, 122, p124508.
-
Kang, J., Jeon, C. W., (2016), “Study on Properties of SnS Thin Films Fabricated by High Temperature Sulfurization”, New. Renew. Ener, 12(1), p31-36.
[https://doi.org/10.7849/ksnre.2016.03.12.1.31]

-
Minami, T., Nishi, Y., Miyata, T., (2016), “Efficiency enhancement using a Zn1-xGex-O thin film as an n-type window layer in Cu2O-based heterojunction solar cells”, Appl. Phys. Express, 9(5), p52301.
[https://doi.org/10.7567/apex.9.052301]

-
Musa, A. O., Akomolafe, T., Carter, M. J., (1998), “Production of cuprous oxide, a solar cell material, by thermal oxidation and a study of its physical and electrical properties”, Sol. Energy. Mater. Sol. Cells, 51(3-4), p305-316.
[https://doi.org/10.1016/s0927-0248(97)00233-x]

-
Mema, R., Yuan, L., Du, Q., Wang, Y., Zhou, G., (2011), “Effect of surface stresses on CuO nanowire growth in the thermal oxidation of copper”, Chem. Phys. Lett, 512(1-3), p87-91.
[https://doi.org/10.1016/j.cplett.2011.07.012]

-
Zou, C. W., Wang, J., Liang, F., Xie, W., Shao, L. X., Fu, D. J., (2012), “Large-area aligned CuO nanowires arrays : Synthesis, anomalous ferromagnetic and CO gas sensing properties”, Curr. Appl. Phys, 12(5), p1349-1354.
[https://doi.org/10.1016/j.cap.2012.03.025]

- Garnett, E. C., Brongersma, M. L., Cui, Y., Mcgehee, M. D., (2011), “Nanowire Solar Cells”, Annu. Rev. Mater. Res, 41, p269-295.
-
Lee, G., (2014), “Large-Scale Synthesis of Cu 2 O Nanowires by Thermal Oxidation Method”, Kor. J. Mater. Res, 24(7), p388-392.
[https://doi.org/10.3740/mrsk.2014.24.7.388]

-
Devan, R. S., Patil, R. A., Lin, J., Ma, Y., (2012), “One-Dimensional Metal-Oxide Nanostructures : Recent Developments in Synthesis, Characterization, and Applications”, Adv. Funct. Mater, 22(16), p3326-3370.
[https://doi.org/10.1002/adfm.201201008]

-
Liao, L., Zhang, Z., Yan, N., Zheng, Z., Bao, Q. L., Wu, T., Li, C. M., Shen, Z., X., Zhang, J. X., Gong, H., Li, J., C., Yu, T., (2009), “Multifunctional CuO nanowire devices : p-type field effect transistors and CO gas sensors”, Nanotechnology, 20(8), p085203.
[https://doi.org/10.1088/0957-4484/20/8/085203]

-
Liu, X., Li, Z., Zhang, Q., Li, F., Kong, T., (2012), “CuO nanowires prepared via a facile solution route and their photocatalytic property”, Mater. Lett, 72, p49-52.
[https://doi.org/10.1016/j.matlet.2011.12.077]

-
Ma, C., Zhu, L., Chen, S., Zhao, Y., (2013), “Simple and rapid preparation of CuO nanowires and their optical properties”, Mater. Lett, 108, p114-117.
[https://doi.org/10.1016/j.matlet.2013.06.101]

-
Lee, D., Kim, D., Kim, H., (2015), “Detection of H2S Gas with CuO Nanowire Sensor”, Kor. J. Mater. Res, 25(5), p238-246.
[https://doi.org/10.3740/mrsk.2015.25.5.238]

-
Cao, L., Park, J., Fan, P., Clemens, B., Brongersma, M. L., (2010), “Resonant Germanium Nanoantenna Photodetectors”, Nano Lett, 10(4), p1229-1233.
[https://doi.org/10.1021/nl9037278]

-
Gunawan, O., Sekaric, L., Majumdar, A., Rooks, M., Appenzeller, J., Sleight, J. W., Guha, S., Haensch, W., (2008), “Measurement of Carrier Mobility in Silicon Nanowires”, Nano Lett, 8(6), p1566-1571.
[https://doi.org/10.1021/nl072646w]

-
Xiang, J., Lu, W., Hu, Y., Wu, Y., Yan, H., Lieber, C. M., (2006), “Ge/Si nanowire heterostructures as highperformance field-effect transistors”, Nature, 441, p489-493.
[https://doi.org/10.1038/nature04796]

-
Xiao, B., Xu, Y., (2011), “VLS synthesis of disordered CdSe nanowires and optical properties of an individual CdSe nanowire”, Physica E, 44(3), p696-699.
[https://doi.org/10.1016/j.physe.2011.11.014]

- Umar, A., Kim, S. H., Lee, Y., Nahm, K. S., Hahn, Y. B. Ã., (2005), “Catalyst-free large-quantity synthesis of ZnO nanorods by a vapor - solid growth mechanism”, J. Cryst. Growth, 282(1-2), p131-136.
-
Yu, L., Lv, Y., Zhang, X., Zhang, Y., Zou, R., Zhang, F., (2011), “Vapor-liquid-solid growth route to AlN nanowires on Au-coated Si substrate by direct nitridation of Al powder”, J. Cryst. Growth, 334(1), p57-61.
[https://doi.org/10.1016/j.jcrysgro.2011.08.025]

-
Kumar, R. R., Rao, K. N., Phani, A. R., (2012), “Growth of silicon nanowires by electron beam evaporation using indium catalyst”, Mater. Lett, 66(1), p110-112.
[https://doi.org/10.1016/j.matlet.2011.08.064]

-
Kuo, B. C., Chen, C., Huang, M. H., (2007), “Seed-Mediated Synthesis of Monodispersed Cu2O Nanocubes with Five Different Size Ranges from 40 to 420 nm”, Adv. Funct. Mater, 17(18), p3773-3780.
[https://doi.org/10.1002/adfm.200700356]

-
Wang, L., Zhang, K., Hu, Z., Duan, W., Cheng, F., Chen, J., (2013), “Porous CuO nanowires as the anode of rechargeable Na-ion batteries”, Nano Res, 7(2), p199-208, ISSN 1738-3935.
[https://doi.org/10.1007/s12274-013-0387-6]