섬유소계 바이오매스로부터 황산 촉매를 이용한 레블린산 생산
Copyright © 2023 by the New & Renewable Energy
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Levulinic acid (LA) derived from cellulosic biomass, serves a crucial intermediate that can be used in various chemical conversions. This study focused on optimizing the production of LA using two types of pretreated rice husk (de-ashed and delignificated cellulosic biomass) in a batch reaction system through catalytic conversion with sulfuric acid. To determine the optimal conditions, the conversions of glucose and α-cellulose were examined to compare the effects of pretreatment on the rice husk. The experimental parameters covered a broad spectrum, including temperatures ranging from 140°C to 200°C, a reaction time was up to 600 minutes, and a substrate to catalyst (acid solution) ratio of 100 g/L. The highest LA yield was 44.8%, achieved from de-ashed rice husk with 3.0 wt.% of sulfuric acid at 180°C and with a reaction time of 180 minutes. In the case of the delignificated rice husk, a LA yield of 43.6% was obtained with 3.0 wt.% of sulfuric acid at 200°C and with reaction time of 30 minutes.
Keywords:
Rice husk, Levulinic aicd, Acid catalytic conversion, Sulfuric acid키워드:
왕겨, 레블린산, 산 촉매 전환, 황산1. 서 론
지속 가능한 화학 산업 및 신재생 에너지에 대한 세계적인 관심이 높아지면서, 바이오매스(biomass), 풍력, 수력 및 태양에너지와 같은 재생 가능한 연구가 확대되고 있다.[1] 이에 대한 배경으로는 2015년도 개최된 파리협정에 따라 2050년까지 전 세계적으로 이산화탄소 배출량을 저감하는 ‘넷제로’에 있다. 기존 석유계 화학제품을 사용함에 있어 지구 온난화 등 지속적인 환경문제가 발생하고 있기 때문에 전 세계적으로 화학제품의 사용을 제한하는 추세이다.[2] 이 가운데 생물자원으로부터 유래된 바이오매스가 석유계 화합물을 대체할 수 있어 현재 바이오 베이스의 화합물 시장이 증가하고 있다.[3] 바이오매스는 옥수수나 사탕수수와 같은 식용작물인 1세대 바이오매스, 리그노 셀룰로오스계 비식용작물인 2세대 바이오매스, 해조류 및 미세 조류와 같은 3세대 바이오매스로 구분된다. 1세대 바이오매스의 경우 식량자원을 사용하기 때문에 생물다양성 및 식량 안보와 관련된 문제를 야기할 수 있다. 2세대 바이오매스는 지구에서 가장 풍부한 에너지 자원으로, 주로 생분해성 섬유소 및 리그닌과 같은 성분을 활용하여 생물 연료, 생화학 연료, 그리고 화력 발전용 연료로 사용되기도 한다. 또한 2세대 바이오매스는 1세대 바이오매스에 비해 곡물 생산과 가격 경쟁력 측면에서 우수하기 때문에 1세대 바이오매스의 단점을 해결할 수 있는 에너지 자원이다.[4] 특히, 섬유소계 바이오매스(cellulosic biomass)는 이러한 연구 분야에서 중요한 역할을 하며, 그중에서도 레블린산(levulinic acid, LA)은 다양한 화학 제품 및 공정에서 활용 가능한 중요한 중간체이다.[5] 예를 들어, 레블린산은 용제, 의약품 및 향미제, 가소제, 바이오 연료/산소 연료 첨가제를 포함한 다양한 바이오 화학 물질을 생산하는 데 사용될 수 있는 플랫폼 화학 물질이다.[6,7]
섬유소계 바이오매스는 농업 폐기물로 얻을 수 있다. 이는 정미 산업의 부산물로서, 쌀껍질의 세계적인 연간 생산량은 약 1억 톤으로 추정되는 인간이 식량으로 사용하지 않는 풍부한 자원이다.[8] 셀룰로오스는 6탄당인 글루코오스(D-glucose)는 β-1,4 glucosidic 결합으로 이루어진 단량체이다. 리그닌(lignin)은 페닐프로판 구조로 이루어진 비정질 중합체로서, 식물 구조에 강성을 주는 역할을 한다.[9] 바이오매스 내 리그닌의 함량이 높으면 글루코오스의 화학반응을 저해시키는 역할도 하기 때문에 섬유소계 바이오매스와 같은 생(生)물질은 리그닌의 함량을 낮추는 전처리 과정이 요구된다.
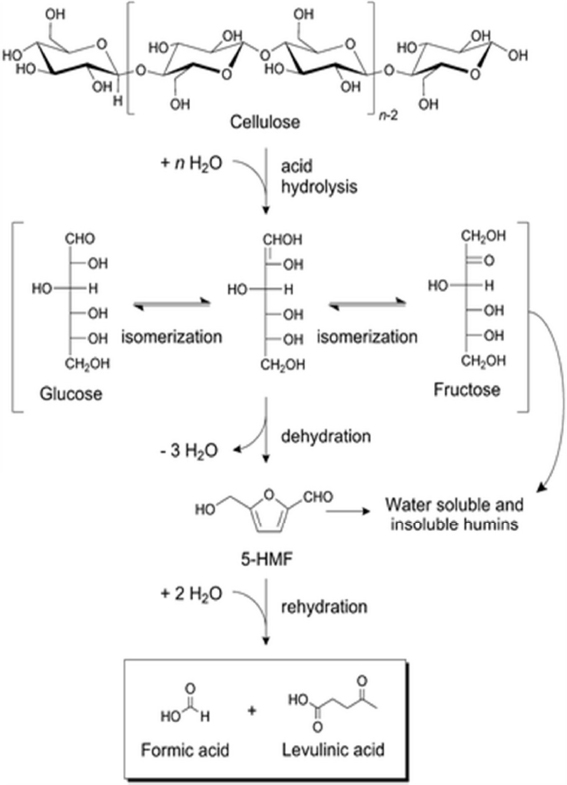
레블린산은 글루코오스로부터 산촉매를 가하여 가수분해를 통해 전환되는 고부가가치 화학물질로, 중간 단계에 많은 화학적 변화가 있지만 크게 Fig. 1과 같은 주요한 화학물질로 반응 경로로 나타낼 수 있다.[10]
셀룰로오스는 산촉매의 존재하에 가수분해 되어 글루코오스로 전환되고, 이성질화 되어 과당이 된 뒤 탈수반응으로 3개의 물분자가 빠지면 5-HMF(5-hydroxymethylfurfural)가 생성된다. 이후 5-HMF가 재수화반응(rehydration)이 일어나서 2개의 물분자가 첨가되면 레블린산이 생성된다.[10,11]
본 연구에서는, α-cellulose와 섬유소계 바이오매스로부터 산촉매 전환공정을 통해 레블린산 생산 공정을 최적화 하였다. 선행연구로는 순수한 시약급 글루코오스로부터 산촉매 전환공정을 통해 얻은 최적 조건과 비교하였다. 선행연구와의 비교를 통해 최적 조건과 본 연구에서 얻은 최적 조건을 비교하였으며 다양한 황산 농도와 온도 조건으로 글루코오스로부터 레블린산을 생산하는 연구를 진행하였다.
2. 실험 재료 및 방법
2.1 재료
본 연구에서 시료로 사용된 D-(+)-글루코오스(D-(+)-glucose,≥99.5%, Cas No. : 50-99-7),알파셀룰로오스(α-cellulose, powder, Cas No : 9004-34-6)는 Sigma-Aldrich Co. (USA)로부터 구입하였으며 organosolv.(에탄올) 전처리 된 바이오매스인 왕겨(de-ashed rice husk, Lot No : CM-FMRH-23035004)는 주식회사 슈가엔(경기도 용인시 수지구 죽전로 152)으로부터 제공받았으며, 염기(NaOH) 전처리된 왕겨(delignificated rice husk)는 한양대(경기도 안산시 상록구 한양대학로 55)로부터 제공받았다. 산촉매로 쓰인 황산(sulfuric acid ≥ 98%, Cas No : 7664-93-9)은 DAEJUNG chemicals & metals로부터 구입하였고, 중화제로 사용된 탄산칼슘(calcium carbonate (extra pure grade) Cas No : 471-34-1)은 DUKSAN PURE CHEMICALS CO.(Korea)로부터 구입하였다.
2.2 방법
본 실험에서 사용된 시료인 글루코오스, α-cellulose 및 섬유소계 바이오매스의 고체성분과 리그닌성분 분석은 NREL(National Renewable Energy Laboratories) procedure(Contract No. DE-AC36-08GO28308; 10.2)에 따라 진행되었다.
글루코오스, α-cellulose, 그리고 전처리 된 섬유소계 바이오매스를 0.1 g±0.0003, 0.5 g±0.0003, 1 g±0.0003을 취해 산촉매 10 ml와 함께 혼합하여, 10 g/L, 50 g/L, 100 g/L로 초기 시료 농도를 설정하였다. 산촉매는 황산(1~3 wt.%)을 사용하였다. 시료의 산촉매 전환 반응을 위해 용적 15 ml, 길이 7.48 in 직경 1/2 in의 회분식 반응기(stainless steel)를 사용하였다. 초기 시료 농도별로 일정량 회분식 반응기에 넣어 오일 중탕기(oil bath)에 투입되어 시간(0~600 min), 반응 온도(140~200°C)에 따라 반응이 진행되었다. 모든 실험은 3회 이상 실시하였으며, 평균값을 구하여 결과를 도출하였다. 또한 각 반응 온도의 pre-heating time(PRT)은 10°C 더 높게 설정하였으며, 140°C의 PRT는 5분 10초, 160°C의 PRT는 4분 50초, 180°C의 PRT는 4분 40초, 200°C의 PRT는 4분 30초 가량 소요된다. 모든 PRT는 오일 중탕기에 반응기가 모두 잠겨있을 때 측정한 것이며, 3회 이상 실험의 평균값으로 나타내었다.
글루코오스, α-cellulose, 그리고 전처리 된 왕겨의 산촉매 탈수 반응 후 취한 시료 용액은 중화를 위해 탄산칼슘(calcium carbonate)를 사용했으며, 고상과 액상의 분리를 위해 14,000 rpm으로 4분간 원심분리기(centrifuge 5415C, eppendorf)를 이용하였다. 분리된 상층 용액은 미세입자를 제거하기 위해 0.22 μm 나일론 시린지 필터를 사용하여 제거하였다. 레블린산은 HPLC(Water, USA)를 이용하여 정량을 진행하였다. 이동상은 5 mM의 황산 용액으로 0.6 ml/min의 유속으로 운전하였다. 분석에 사용된 column은 Bio-rad 사의 Aminex HPX-87H(300 × 7.8 mm)를 사용하였고, detector로는 Waters 410 RI(refractive index)를 사용하였다. 칼럼(column)과 RI검출기의 온도는 각각 60°C와 50°C로 설정되었다. 글루코오스, α-cellulose, 그리고 전처리 된 섬유소계 바이오매스의 전환율은 식 (1)을 이용하여 계산하였고, 레블린산의 생성수율은 식 (2)을 이용하였다.[11]
| (1) |
| (2) |
3. 실험결과
3.1 글루코오스로부터 레블린산 최적 생산
글루코오스는 레블린산 생산의 가장 기본적인 원료로, 주로 황산 촉매를 이용하여 높은 수율로 레블린산을 생산할 수 있다. 초기 글루코오스 농도를 100 g/L 기준으로 하였으며, 글루코오스로부터 레블린산을 생산하기 위한 최적 조건을 확인하고자 Table 1에 나타낸 바와 같이 황산 촉매농도는 1~3 wt.%, 반응 온도는 140~200°C로 변화를 주어 반응시켰다.
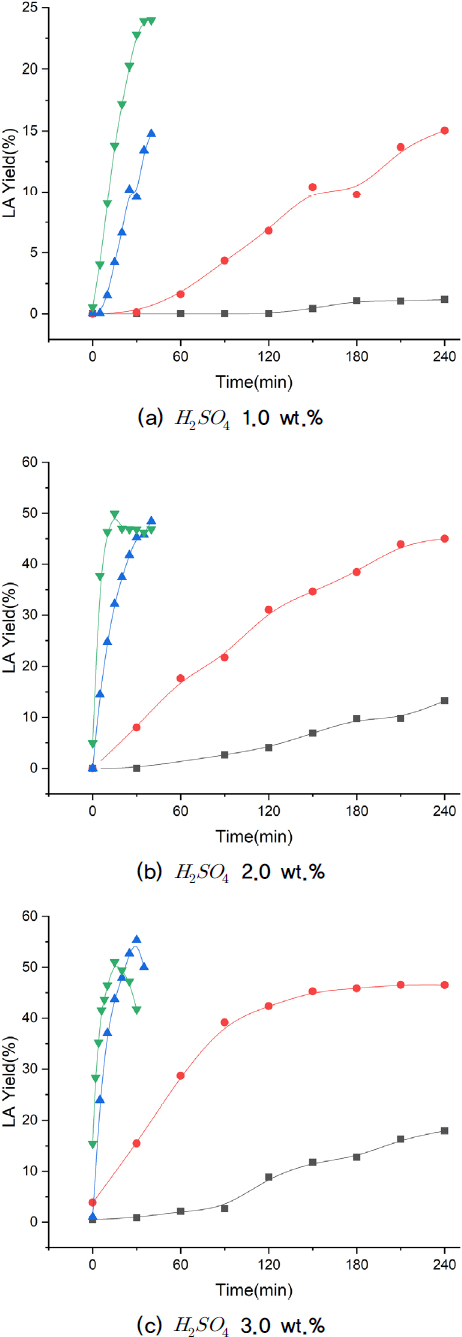
Fig. 2의 (a)~(c)는 황산 촉매 1~3 wt.% 일 때, 온도에 따른 레블린산 수율을 나타낸 그래프이다. 반응온도와 황산촉매의 농도를 높일수록 레블린산의 생성 속도가 증가하였으며, 온도가 140°C에서 200°C로 증가하면서, 반응시간이 30분일 때 레블린산 수율이 1.16%에서 46.4%로 증가하였다.
온도가 증가할수록 레블린산의 생성이 빠르게 일어났지만(Fig. 2의 (a)), 레블린산의 수율은 황산 촉매 농도 2~3 wt.%(Fig. 2의 (b), (c))에 비해 낮다. 이는 황산 촉매의 농도가 레블린산의 생성 농도에 큰 영향을 주며 더 높은 농도의 레블린산 수율을 확보하려면 더 긴 반응시간을 주어야하기 때문에 공정상 1.0 wt.%는 비효율적이라 판단된다.
Fig. 2의 (b)와 (c)에서 글루코오스 전환이 비교적 빠른 시간 내에 일어났으며 레블린산의 최대 전환 수율을 얻었다. 온도에 따른 레블린산의 생성은 비슷한 경향이 나왔지만 황산 촉매 2.0 wt.% 보다 3.0 wt.% 조건에서 레블린산의 수율이 더 높았으며 이때 레블린산의 전환 수율은 55.4%이다.
낮은 온도(140°C)에서 글루코오스의 전환이 다 이루어지지 않았으며 레블린산의 수율은 긴 시간을 반응시켜도 비교적 낮은 수율이 나왔다. 높은 온도(180~200°C)에서는 글루코오스는 빠르게 전환되고 레블린산의 농도는 30 min 전후로 높은 농도를 생성하다가 떨어지는데, 이는 레블린산의 생성 속도보다 분해되는 속도가 더 빠르다는것을 의미하며, 최대 레블린산 생성 온도와 촉매 농도는 180°C, 황산촉매 3.0 wt.% 조건이 적절하다고 판단된다. 각 조건에 따른 레블린산의 최대 수율은 Table 2에 나타내었다.
3.2 α-cellulose로부터 레블린산 최적 생산
셀룰로오스는 바이오매스의 주요 구성 성분으로, 글루코오스로 가수분해 되고 탈수분해를 통해 레블린산으로 전환될 수 있다. α-cellulose의 고체성분 및 리그닌 분석의 실험 결과, 글루코오스(79.9%), 헤미셀룰로오스(20.1%)가 함유된 리그닌이 없는 정제된 바이오매스이다. α-cellulose는 글루코오스가 올리고머(oligomer)의 형태로 존재한 분자량의 범위가 매우 넓은 바이오매스로, 분자량을 특정 짓기에는 한계가 있지만 raw biomass와 순수한 시약급 글루코오스 사이에 존재하는 과도기적인 바이오매스라고 판단되어 선행연구로 택하였다.
반응온도, 반응시간, 촉매 농도 조건은 Table 2에 나타내었으며 온도에 따른 레블린산 생성수율을 Fig. 3에 나타내었다.
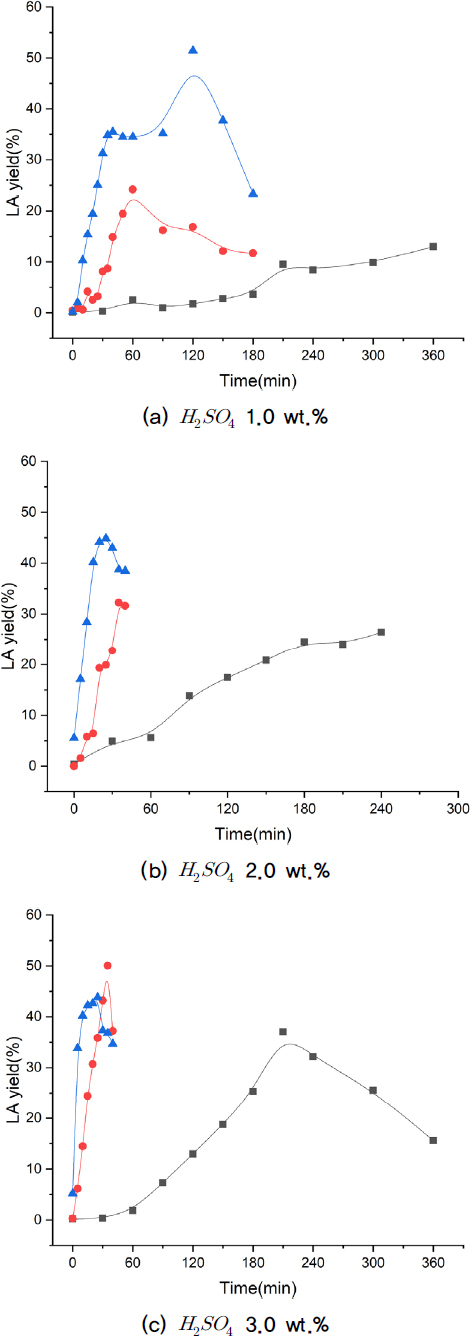
Fig. 3의 (a)~(c)는 황산 촉매 1~3 wt.% 일 때, 온도에 따른 레블린산의 생성수율을 나타낸 그래프이다. 반응온도와 황산촉매의 농도가 증가할수록 레블린산 생성속도가 증가하는 경향이 나왔다.
반응시간 120 min, 반응온도 200°C 구간(a)에서 레블린산의 최대 전환수율 51.5% 확보하였다. 160°C와 180°C의 온도는 글루코오스에서 레블린산으로 가기위한 에너지에 비해 촉매의 농도가 낮아 200°C보다 더 긴 반응시간이 필요하다.
반응시간 35 min, 반응온도 180°C 구간(c)에서 레블린산의 최대 전환수율 50.1% 확보하였다.
그래프를 통해 α-cellulose의 반응 최적 온도와 촉매는 180°C에서는 산 농도 3.0 wt.%, 200°C에서는 1.0 wt.%임을 확인하였다. Fig. 3의 (a)에서 반응온도가 160°C일 때 레블린산의 생성수율이 계속 증가하고 있는 경향이 있지만, 너무 많은 반응시간이 필요하기 때문에 더 효율적인 공정으로 운용하려면 산 농도 3.0 wt.%에서 반응온도를 낮추고, 반응시간을 비교적 더 짧게 끌고간 180°C 조건이 적합하다고 판단된다.
3.3 Rice husk biomass로부터 레블린산 최적 생산
섬유소계 바이오매스는 셀룰로오스뿐만 아니라 헤미셀룰로오스와 리그닌도 함유하고 있으며, 이들은 레블린산 합성에 영향을 미칠 수 있다. 본 연구에서는 섬유소계 바이오매스로서 왕겨(rice husk)를 사용하였다. 주식회사 슈가엔으로부터 제공받은 왕겨는 organosolv 전처리된 바이오매스로 셀룰로오스(90.7%), 헤미셀룰로오스(2.5%), 리그닌(6.8%)를 함유하고 있다. 한양대(Erica) 에서 제공받은 왕겨는 NaOH 전처리된 바이오매스로 셀룰로오스(64.9%), 헤미셀룰로오스(27.5%), 리그닌(7.6%)를 함유하고 있다. 두 왕겨섬유를 기존 글루코오스와 α-cellulose의 레블린산의 생성수율에서 확인한 최적조건인 180°C와 200°C, 촉매농도 3.0 wt.%의 조건으로 실험을 진행하고 레블린산의 최대 전환수율을 비교하고자 한다.
주식회사 슈가엔으로부터 제공받은 왕겨는 organosolv인 ethanol을 첨가하여 리그닌과 헤미셀룰로오스도 제거하지만 주로 ash를 제거한 바이오매스이다.
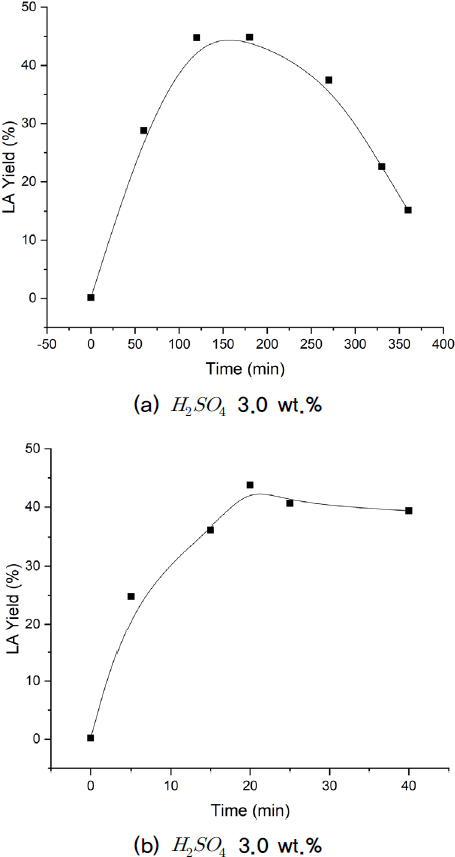
Fig. 4의 (a), (b)는 산 촉매 3.0 wt.% 일 때, 온도 180°C와 200°C에 따른 레블린산의 수율을 나타낸 그래프이다.
반응시간 180 min, 반응온도 180°C 구간(a)에서 레블린산의 최대 전환수율 44.8%를 확보하였다.
반응시간 20 min, 반응온도 200°C 구간(b)에서 레블린산의 최대 전환수율 43.76%를 확보하였다.
결과적으로 최대 레블린산 수율을 얻기위한 최적 조건은 180°C, 산촉매 3.0 wt.%로, 이때 레블린산의 최대 전환수율은 44.8%로 나타났다.
한양대(Erica)에서 제공받은 섬유소계 바이오매스는 NaOH를 첨가하여 주로 바이오매스의 구성성분인 리그닌을 제거하여 제공받았다.
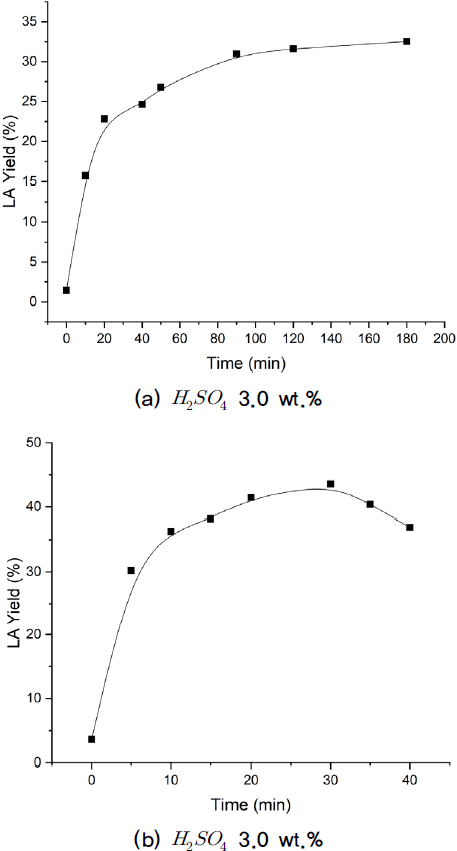
Fig. 5의 (a)와 (b)는 산 촉매 3.0 wt.% 일 때, 온도 180°C와 200°C에 따른 레블린산의 생성수율을 나타낸 그래프이다.
반응온도 180°C, 산 촉매 3.0 wt.%에 대한 조건(a)은 반응시간이 180 min 에서도 레블린산의 최대 전환수율은 32.5%이다. 기존 글루코오스와 α-cellulose의 경향으로 확인해보았을 때 탈리그닌 처리된 바이오매스는 반응시간 180 min 이후의 경우 필요한 에너지, 시간 등 공정상 대체적으로 효율적이지 않다고 판단된다.
반응시간 30 min, 반응온도 200°C 구간(b)에서 레블린산의 최대 전환수율 43.6%를 확보하였다.
3.4 최적 조건에서 기질에 따른 글루코오스 전환율 비교
Fig. 6은 최적 조건에서의 글루코오스의 전환율을 나타낸 그림이다. 글루코오스의 최적 조건인 반응온도 180°C, 산 농도 3.0 wt%, 반응시간 30 min에서의 글루코오스의 전환율은 0.9%로 거의 다 전환된 것으로 확인되었다.
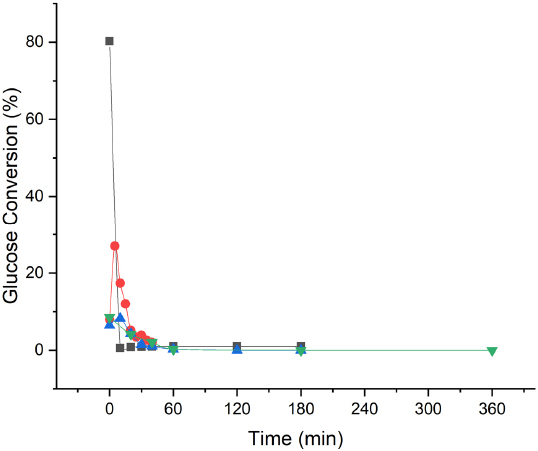
Glucose Conversion (%) at temperature 180°C, H2SO4 3.0 wt.% (■ Glucose, ● α-cellulose, ▲ De-lignin biomass, ▼ De-ashed biomass)
α-cellulose의 최적 조건인 반응온도 180°C, 산 농도 3.0 wt.%, 반응시간 35 min에서의 글루코오스의 전환율은 2.6%로 아직 다 전환되지 않은 것으로 확인되었으며, 이는 추가적인 실험을 통해 레블린산의 수율을 더 높일 수 있을 것으로 판단된다.
탈회분 바이오매스의 최적 조건인 반응온도 180°C, 산농도 3.0 wt.%, 반응시간 180 min 에서의 글루코오스 전환율은 0%로 모두 전환된 것을 확인하였다.
마지막으로 탈리그닌 바이오매스의 최적 조건인 반응온도 200°C, 산 농도 3.0 wt.%, 반응시간 30 min에서의 글루코오스 전환율은 0%로 마찬가지로 모두 전환된 점을 확인하였다.
바이오매스에서 레블린산으로 전환되는 반응은 셀룰로오스에서 글루코오스, 글루코오스에서 레블린산으로 반응이 이루어지기 때문에 본 연구에서 확인된 최적 조건인 반응온도 180°C와 200°C, 산 농도 3.0 wt.%에서 글루코오스가 모두 전환되었는지 확인하였다. 최적 조건에서 글루코오스가 다 전환되지 않았다는 것은 아직 레블린산으로 반응이 더 이루어질 수 있다는 뜻이기 때문에 글루코오스의 전환율을 확인하는 것은 중요하다.
3.5 최적 조건에서 기질에 따른 LA yield 비교
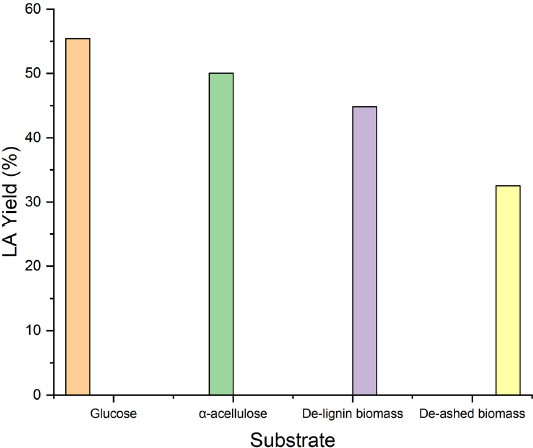
Fig. 7은 반응온도 180°C, 산 농도 3.0 wt.%에서 각 바이오매스의 레블린산 최대 전환수율을 나타낸 막대그래프이다. 글루코오스에서 α-cellulose, 그리고 전처리된 섬유소계 바이오매스로 갈수록 레블린산의 최대 전환수율이 감소하는 경향이 나타난다. 이러한 이유로는 바이오매스의 경우 리그닌이 존재하기 때문에 리그닌에 흡착되는 효소의 증가와 같은 효과 때문에 화학적 저해 반응이 일어나기 때문이다.[12,13] Fig. 7에서도 볼 수 있듯 탈리그닌 바이오매스의 경우가 탈회분 바이오매스보다 레블린산의 최대 전환수율이 더 높은 것으로 확인된다.
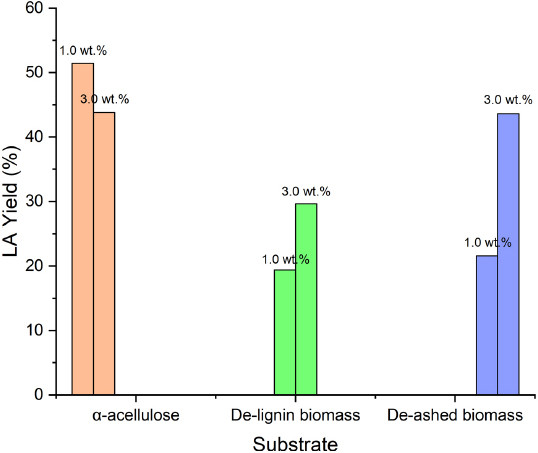
Fig. 8은 반응온도 200°C, 산 농도 1.0 wt.%와 3.0 wt.%에서 α-cellulose와 섬유소계 바이오매스의 레블린산 최대 전환수율을 나타낸 막대그래프이다. α-cellulose는 리그닌을 함유하고 있지 않기 때문에 화학적 저해 반응으로 인한 레블린산 수율의 감소가 적다. 그래서 반응온도 200°C 조건에서는 산 농도를 세게 가하는 것보다 낮은 농도로 반응시간을 길게 가하는 것이 레블린산의 최대 전환수율이 더 높다는 것이 확인 가능하다. 반면, 같은 온도 조건에서 섬유소계 바이오매스의 경우는 리그닌뿐만 아니라 무기질 물질의 잔여물인 ash를 함유하고 있기 때문에 기타 부반응이 일어날 수 있다. 따라서 Fig. 8에서와 같이 탈리그닌 바이오매스의 경우보다 탈회분 바이오매스가 부반응에 의한 byproduct의 생성이 더 적기 때문에 반응온도와 산의 세기를 높였을 때 레블린산의 최대 전환수율이 더 높은 것을 확인할 수 있다.
4. 결 론
본 연구에서는 섬유소계 바이오매스로부터 황산 촉매를 사용하여 레블린산을 생산하는 최적 조건을 확인하는 연구를 진행하였다. 비교군을 두기 위하여 시약급 글루코오스와 α-cellulose의 실험 결과를 확인하였으며, 반응시간, 산 농도, 반응온도 등의 변수에 따른 결과값을 참고하여 최적조건을 도출하였다.
온도와 산 농도가 증가함에 따라 레블린산의 최대 전환수율은 더 높아질 수 있겠지만, 온도를 증가시킴에 따라 드는 에너지와 비용이 증가하며, 산 촉매로 황산을 사용했기 때문에 농도를 증가시킴에 따라 장비의 부식 정도가 더 심해지기 때문에 적절하지 않다고 판단된다.
따라서 상업적인 목적을 고려하였을 때 가장 적절한 바이오매스는 탈회분 바이오매스를 기질로 사용한 180°C의 온도와 촉매는 황산 촉매 3.0 wt.%이며, 100 g/L의 바이오매스 초기 농도에서 레블린산 생산의 최적 조건이라고 판단된다.
Nomenclature
| XGlu : | conversion of glucose |
| YLA : | yield of levulinic acid |
Subscript
| LA : | levulinic acid |
Acknowledgments
본 연구는 산업통산자원부의 ‘MTHF 생산을 위한 중간체(르블린산, 퍼퓨랄 등) 생산 기술 개발’의 일환으로 수행되었습니다(과제 번호 : RS-2022-00156181).
References
-
Lakshmanan, V.I. and Gorain, B., 2019, “Innovations and breakthroughs in the gold and silver industries: Concepts, applications and future trends”, 1st ed. Springer, New York.
[https://doi.org/10.1007/978-3-030-32549-7]

-
Fankhauser, S., Smith, S.M., Allen, M., Axelsson, K., Hale, T., Hepburn, C., Kendall, J.M., Khosla, R., Lezaun, J., and Mitchell-Larson, E., et al., 2022, “The meaning of net zero and how to get it right”, Nature Climate Change, 12, 15-21.
[https://doi.org/10.1038/s41558-021-01245-w]

-
Nikolau, B.J., Perera, M.A.D.N., Brachova, L., and Shanks, B., 2008, “Platform biochemicals for a biorenewable chemical industry”, The Plant Journal, 54(4), 536-545.
[https://doi.org/10.1111/j.1365-313X.2008.03484.x]

- Kim, J.S., Lee, S.M., and Han, S.J., 2023, “Levulinic acid production from lignocellulosic biomass by co-solvent pretreatment with NaOH/THF”, Korean Chem. Eng. Res., 61(2), 265-272.
-
Rackemann, D.W., and Doherty, W.OS., 2011, “The conversion of lignocellulosics to levulinic acid”, Biofpr, 5(2), 198-214.
[https://doi.org/10.1002/bbb.267]

-
Bozell, J., Moens, L., Elliott, D.C., Wang, Y., Neuenscwander, G.G., Fitzpatrick, S.W., Bilski, R.J., and Jarnefeld, J.L., 2000, “Production of levulinic acid and use as a platform chemical for derived products”, Resour Conserv Recycl., 28(3-4), 227-239.
[https://doi.org/10.1016/S0921-3449(99)00047-6]

-
Campbell, G.M., Webb, C., and McKee, S.L., 1997, “Cereals: Novel uses and processes”, Plenum Press, New York and London.
[https://doi.org/10.1007/978-1-4757-2675-6]

-
Williams, P.T., and Nugranad, N., 2000, “Comparison of products from the pyrolysis and catalytic pyrolysis of rice husks”, Energy, 25(6), 493-513.
[https://doi.org/10.1016/S0360-5442(00)00009-8]

-
Alonso, D.M., Bond, J.Q., and Dumesic, J.A., 2010, “Catalytic conversion of biomass to biofuels”, Green Chem., 12, 1493-1513.
[https://doi.org/10.1039/c004654j]

-
Van de Vyver, S., Thomas, J., Geboers, J., Keyzer, S., Smet, M., Dehaen, W., Jacobs, P.A., and Sels, B.F., 2011, “Catalytic production of levulinic acid from cellulose and other biomass-derived carbohydrates with sulfonated hyperbranched poly (arylene oxindole)s”, Energy Environ. Sci., 4, 3601-3610.
[https://doi.org/10.1039/c1ee01418h]

- Han, S.J., Lee, S.M., and Kim, J.S., 2022, “Kinetic study of glucose conversion to 5-hydroxymethylfurfural and levulinic acid catalyzed by sulfuric acid”, Korean Chem. Eng. Res., 60(2), 193-201.
-
Shi, N., Liu, Q., Cen, H., Ju, R., He, X., and Ma, L., 2020, “Formation of humins during degradation of carbohydrates and furfural derivatives in various solvents”, Biomass Convers. Biorefin., 10(2), 277-287.
[https://doi.org/10.1007/s13399-019-00414-4]

-
Ban, S.E., Park, Y., Yi, S.C, Lim, Y.E., and Lee, J.W., 2021, “Production of levulinic acid using glucose derived from office waste paper”, New. Renew. Energy, 17(2), 32-39.
[https://doi.org/10.7849/ksnre.2021.0005]