Plug Flow Reactor 모델을 이용한 폐플라스틱의 열분해 특성 해석
Copyright © 2022 by the New & Renewable Energy
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
The pyrolysis characteristics of high-density polyethylene (HDPE), low-density polyethylene (LDPE), and polypropylene (PP) were analyzed numerically using a 1D plug flow reactor (PFR) model. A lumped kinetic model was selected to simplify the pyrolysis products as wax, oil, and gas. The simulation was performed in the 400-600°C range, and the plastic pyrolysis and product generation characteristics with respect to time were compared at various temperatures. It was found that plastic pyrolysis accelerates rapidly as the temperature rises. The amounts of the pyrolysis products wax and oil increase and then decrease with time, whereas the amount of gas produced increases continuously. In LDPE pyrolysis, the pyrolysis time was longer than that observed for other plastics at a specified temperature, and the amount of wax generated was the greatest. The maximum mass fraction of oil was obtained in the order of HDPE, PP, and LDPE at a specified temperature, and it decreased with temperature. Although the 1D model adopted in this study has a limitation in that it does not include material transport and heat transfer phenomena, the qualitative results presented herein could provide base data regarding various types of plastic pyrolysis to predict the product characteristics. These results can in turn be used when designing pyrolysis reactors.
Keywords:
Pyrolysis, High density polyethylene, Low density polyethylene, Polypropylene, Plug flow reactor, Lumped kinetic model키워드:
열분해, 고밀도 폴리에틸렌, 저밀도 폴리에틸렌, 폴리프로필렌, 플러그 반응기, 집중 반응속도 모델1. 서 론
최근 플라스틱의 사용량 증가에 따라 플라스틱 폐기물 발생량 역시 지속적으로 증가하고 있다. 폐플라스틱을 재활용하는 방법은 크게 세 가지로 구분할 수 있으며, 물리적 재활용(material recycling), 화학적 재활용(chemical recycling), 열적 재활용(thermal recycling) 방법이 있다.[1,2] 물리적 재활용은 폐플라스틱을 종류별로 선별하고 기계적인 방법으로 분쇄, 성형하여 플레이크(flake) 또는 펠릿(pellet) 등을 이용한 재생 플라스틱 제품을 생산하는 방법이다. 그런데 플라스틱 제품은 단일재질보다는 다양한 용도로 복합재질이 사용되는 경우가 많고 폐기물로 배출되는 경우에는 이물질이 함유된 경우가 많기 때문에, 물리적인 재활용의 경우 품질이 저하될 가능성이 많아 활용 분야에 한계가 있다. 열적 재활용은 직접 연소, 고형연료화,[3,4] 가스화[5] 등을 통하여 연료로 활용하는 방법으로 물리적 재활용에 비해서는 많은 전처리가 요구되지는 않지만 최근 대두되고 있는 탄소중립에 부합하기는 어렵기 때문에 열적 재활용의 비율은 가능한 낮추는 것이 바람직할 것으로 보인다. 화학적 재활용은 고체상의 폐플라스틱을 열화학적 방법을 통하여 액체상의 오일로 전환하고 이를 기존의 석유화학 원료를 대체할 수 있는 물질로 활용하는 방법으로, 여러 가지 재질의 플라스틱이 혼합된 경우에도 적용 가능한 장점이 있어 최근 많은 관심을 받고 있다.
폐플라스틱의 화학적 재활용 방법은 고체상의 폐플라스틱을 무산소 분위기에서 열분해하여 기체상의 열분해가스를 생성하고, 이 열분해가스를 응축하여 오일로 전환하는 과정이며 생산된 열분해오일은 추가적인 분리 또는 크래킹 공정을 통하여 화학원료로 사용될 수 있다. 폐플라스틱을 열분해하기 위한 반응기로는 로터리 킬른식, 유동층식, 스크류 방식 등 다양한 형태의 반응기가 개발되고 있으며 반응기 내 코킹이나 고비점 왁스 생성에 의한 문제점을 해결하기 위한 노력이 이루어지고 있다.
열분해반응기의 설계 및 운전 최적화를 위해서는 폐플라스틱의 열분해 특성 및 생성물 분포를 예측하는 것이 중요하며, 이를 위하여 적절한 열분해 반응속도 모델링(pyrolysis kinetic modeling)을 적용하여 플라스틱의 열분해 과정을 모사하는 연구가 수행되고 있다.[6~26] 반응속도 모델링 방법은 크게 메커니즘 기반 반응속도 모델(mechanistic kinetic model), 총괄 반응속도 모델(global kinetic model), 집중 반응속도 모델(lumped kinetic model) 방법이 있다. 메커니즘 기반 모델은 고분자 플라스틱의 열분해 과정을 initiation, hydrogen abstraction, β-scission and termination 등의 단계로 세분화하여 각각의 반응속도 상수를 도출하는 방법으로, 열분해 생성물을 상세하게 모사할 수 있는 장점이 있으나 수백~수천 개의 화학종 및 수만 단계의 화학반응으로 이루어져 있어 추후 전산유체역학(CFD)를 통한 반응기 해석에 적용하기에는 한계점이 있다. 총괄 반응속도 모델링은 열분해반응을 한 단계의 화학반응으로 표현하는 방법으로, 주로 열중량 분석법(thermogravimetric analysis, TGA)을 이용하여 반응 차수(n, reaction order), 활성화에너지(Ea, activation energy), 지수 앞 인자(A, pre-exponential factor)를 도출할 수 있다. 이 방법은 열분해 과정을 단순하게 표현할 수 있는 장점이 있으나 다양한 열분해 생성물을 모사할 수 없는 단점이 있다. 집중 반응속도 모델은 다양한 성분의 열분해 생성물을 유사한 성질의 묶음으로 구성된 몇 종류의 lumped species로 표현하는 방식으로, 10종류 내외의 화학종 및 반응식으로 열분해반응을 모사하고 생성물을 예측할 수 있는 장점이 있다.
본 연구에서는 plug flow reactor(PFR) 모델을 이용하여 실제 열분해반응기 모사에 대한 적용 가능성을 도출해 보고자 하였다. 추후 열분해반응기에 대한 전산유체역학(CFD) 해석 적용 가능성을 고려하여, 다양한 선행 연구에서 제시된 집중 반응속도 모델(lumped kinetic model) 중에서 폐플라스틱 종류 중 가장 많은 비중을 차지하는 폴리에틸렌(polyethylene, PE) 및 폴리프로필렌(polypropylene, PP)의 열분해반응 모사에 적합한 모델을 선정하였다. 플라스틱 종류, 반응온도, 체류시간 등 다양한 조건에 따른 열분해 속도 및 생성물을 비교하였다.
2. 해석 방법
2.1 Plug flow reactor 모델
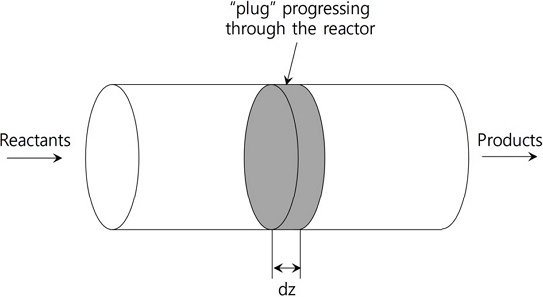
Plug-flow reactor(PFR)는 Fig. 1에 나타낸 것과 같이 일정한 단면적을 가지는 1차원적인 반응기로, 한쪽에서 반응물이 공급되어 반대쪽 방향으로 진행하면서 화학반응이 진행된다. 내부 화학반응 및 화학종 분포는 축방향으로만 변화가 있으며, 반경 방향으로는 모두 균일한 것으로 가정한다. Plug-flow reactor 모델은 주로 점화지연시간(ignition delay time), 배출물 특성, 촉매반응 등을 모사하는 데 널리 사용된다. 본 연구에서는 오픈소스 소프트웨어인 Cantera[27] 를 이용하여 PFR 모델링을 수행하였다.
PFR에 대한 지배방정식은 다음과 같이 연속방정식, 화학종 방정식, 에너지 방정식, 운동량 방정식으로 구성된다.
| (1) |
| (2) |
| (3) |
| (4) |
여기에서 u는 축방향 속도(m/s), P’는 화학적 활성 둘레(m), U는 열전달 계수(W/m/K), P는 반응기 둘레, Tw는 벽면 온도(K), τw는 벽 마찰계수이다. 위의 지배방정식처럼 PFR 모델은 1차원 형상을 가지고 있으나, 확산 현상을 무시하기 때문에 반응기 후류는 상류에 영향을 미치지 않으며 이에 따라 연속적인 0D CSTR 반응기(continuously stirred tank reactor)들로 모사할 수 있으며 Cantera에서는 이러한 방법을 적용하여 PFR 해석을 수행하게 된다. CSTR 에 대한 연속방정식, 화학종 방정식, 에너지 방정식은 각각 다음과 같다.
| (5) |
| (6) |
| (7) |
2.2 반응속도 모델
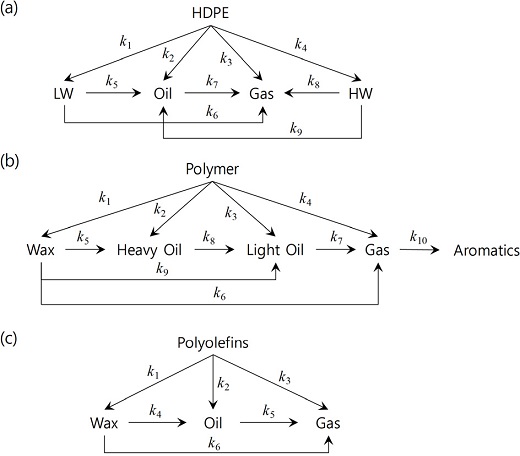
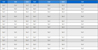
고밀도 폴리에틸렌(HDPE), 저밀도 폴리에틸렌(LDPE), 폴리프로필렌(PP)의 열분해 반응속도론에 대하여 다양한 lumped kinetic model이 제시되고 있다. Eidesen et al.[22]은 Fig. 2(a)에서와 같이 HDPE 열분해 반응물을 크게 light wax, oil, gas, heavy wax로 분류하고 420℃의 온도에서 반응속도 상수(k)를 도출하였는데, 활성화에너지(Ea) 및 지수 앞 인자(A)를 별도로 제시하지는 않았다. Kulas et al.[25]은 micropyrolysis reactor에서 HDPE, LDPE, PP의 열분해실험을 550℃-600℃의 온도범위에서 수행하고 Fig. 2(b)에서와 같이 열분해 생성물을 wax, heavy oil, light oil, gas, aromatics 로 분류하여 각 반응에 대한 활성화에너지(Ea) 및 지수 앞 인자(A)를 도출하였다. Jiang et al.[26]은 tube reactor에서 HDPE, LDPE, PP의 열분해실험을 450℃-550℃의 온도범위에서 수행하고 Fig. 2(c)에서와 같이 열분해 생성물을 wax, oil, gas 로 분류하였으며, 6개의 1차 반응에 대한 활성화에너지(Ea) 및 지수 앞 인자(A)를 도출하였다. 본 연구에서는 Jiang et al.[26]이 제시한 반응속도 인자를 적용하여 PFR 해석을 수행하였다. 각 플라스틱 종류별 반응속도인자를 Table 1에 정리하였다.
3. 결과 및 고찰
3.1 플라스틱 종류별 열분해 특성
PFR 모델링에 대한 플라스틱 종류 및 반응온도, 체류시간 등의 해석 조건을 Table 2에 정리하였다. PFR 모델링은 400, 450, 500, 550, 600℃의 등온 조건에서 수행하였고, 각 온도에서 시간에 따른 플라스틱의 열분해 특성 및 왁스, 오일, 가스의 생성 특성을 비교하였다. 플라스틱 종류 및 온도에 따라 열분해에 소요되는 시간은 매우 차이가 크기 때문에, 반응기 내 체류시간은 플라스틱의 질량 분율이 0에 수렴한 이후 충분한 시간으로 설정하였다. 설정된 최대 체류시간 이후에도 생성물의 분율이 변화할 수 있으나, 열분해의 주요 목적을 오일 생산으로 보았을 때를 가정하여 최대 오일 분율을 얻을 수 있는 시간에 도달한 후 일정 시간까지만을 주요 해석 영역으로 하였다. 이후 분석 그래프상에서는 시간에 따른 열분해 특성 비교를 위하여 모두 동일한 시간 스케일에서 분석하였다.
Fig. 3은 450℃의 온도에서 시간에 따른 HDPE, LDPE, PP의 열분해 및 생성물 변화를 나타낸다. 세 종류의 플라스틱 모두 초반에 급격히 분해되다가 서서히 느려진다. 열분해 생성물인 왁스와 오일은 공통적으로 시간에 따라 증가하였다가 감소하고, 가스는 지속적으로 증가한다. 각 생성물의 시간에 따른 변화는 플라스틱 종류에 따라 다른 특성을 보인다.
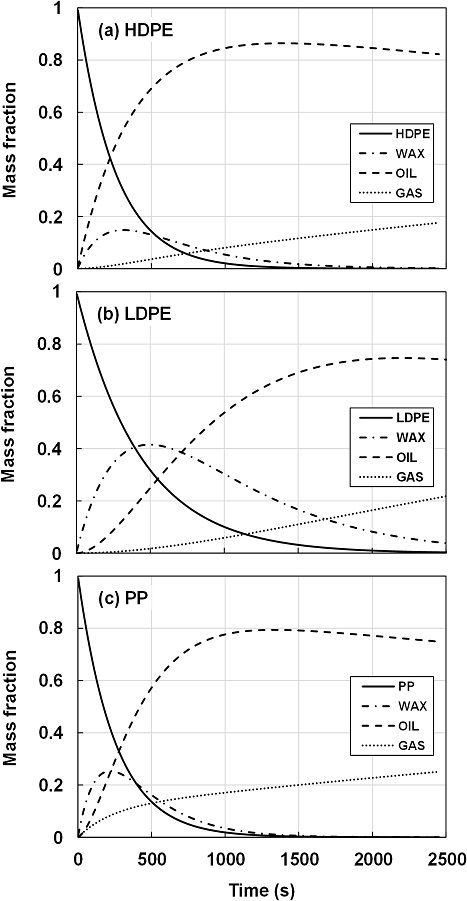
Mass fractions of feedstock and pyrolysis products with time for (a) HDPE, (b) LDPE and (c) PP at 450°C
HDPE의 열분해 생성물 중 오일은 Fig. 3(a)에서와 같이 가장 먼저 생성되기 시작하여 1,400초 근처에서 최대가 되었다가 서서히 감소한다. 왁스는 300초 근처에서 최대가 되었다가 감소하며, 가스는 초반에 서서히 생성되다가 거의 선형적으로 증가한다. 시간에 따른 가스의 분율 변화로 보았을 때, 가스는 플라스틱의 열분해에 의하여 직접 생성되는 것보다는 왁스 또는 오일의 2차 분해에 의하여 주로 생성되는 것으로 생각된다.
LDPE의 열분해는 Fig. 3(b)에서와 같이 HDPE에 비하여 느리게 발생한다. 또한 왁스가 오일보다 먼저 생성되기 시작하여 500초 근처에서 최대가 되는데, 그 최대값은 HDPE의 경우에 비하여 약 2.8배 크다. 오일은 2,200초 근처에서 최대가 되고, 그 최대값은 HDPE보다 작다. 가스의 생성 특성은 HDPE의 경우와 큰 차이를 보이지는 않는다. PP의 열분해는 Fig. 3(c)에서와 같이 HDPE와 전반적으로 유사한 특성을 가지는데, HDPE에 비해서는 초반에 왁스가 먼저 생성되기 시작하고 가스의 생성도 다소 빠르게 발생하는 차이가 있다.
플라스틱 종류에 따른 열분해 속도를 기존의 선행 연구 결과와 비교하여 보았을 때, PP의 경우 1, 2차 탄소보다 3차 탄소의 개수가 PE에 비하여 많고, 3차 탄소를 포함하는 사슬의 분해가 1차 또는 2차 탄소에 비하여 잘 일어나기 때문에[26] 일반적으로 PP의 열분해가 PE에 비하여 빨리 일어나는 것으로 알려져 있다.[25,28,29] 선행 연구[28]에서 제시된 플라스틱의 열중량 분석 결과를 구체적으로 살펴보면, 400℃ 이하의 상대적으로 저온 영역에서 PP의 분해가 PE에 비하여 활발히 진행되는 것을 알 수 있다. Fig. 3에서 HDPE와 PP의 열분해 생성물인 오일의 변화만을 비교해 본다면 HDPE의 오일 생성이 PP보다 빨리 진행되지만, HDPE와 PP 원시료의 열분해 곡선을 비교해 보면 PP의 분해가 약간 더 빨리 진행되어 알려진 것과 일치하는 것을 알 수 있다. 왁스의 경우 초기 생성은 PP가 HDPE에 비하여 많지만, PP에서 생성되는 왁스는 시간이 경과하면서 분해되어 오일 및 가스로 전환되는 속도가 HDPE에서보다 더 빠르기 때문에 667초 이후에는 HDPE의 왁스가 더 많아지게 된다. 따라서, 각각의 생성물 분율은 체류시간에도 많은 영향을 받는 것으로 판단된다. 다양한 온도에서 각 플라스틱의 열분해 특성은 다음 절에서 상세히 비교하였다.
3.2 온도에 따른 플라스틱의 열분해 특성
Fig. 4는 400℃-600℃의 온도에서 각 온도에 대한 HDPE의 열분해 및 각 생성물의 시간에 따른 변화를 나타낸다. HDPE의 분해는 Fig. 4(a)에서와 같이 온도가 증가하면서 급격히 빨라진다. 왁스는 Fig. 4(b)에서와 같이 각 온도에서 열분해 초반에 빠르게 증가하여 최대값에 도달하였다가 이후 서서히 감소하는데, 그 최대값은 온도 증가에 따라 약간씩 증가하는 특성이 있다. 오일 또한 Fig. 4(c)에서와 같이 증가하였다가 감소하는데 최대값에 도달하는 시점은 왁스보다 늦게 나타나며, 그 최대값은 온도에 따라 감소한다. Fig. 4(d)에 나타난 가스의 생성은 온도 증가에 따라 급격히 빨라진다. Fig. 4(c), (d)에서 오일과 가스의 분율은 Table 2에서 설정한 최대 체류 시간까지만 계산되었기 때문에, 그 이후의 값은 그래프상에 존재하지 않지만 그 변화의 추이를 보았을 때 시간이 더 경과하면 오일은 지속적으로 감소하고 가스는 증가할 것으로 보인다.
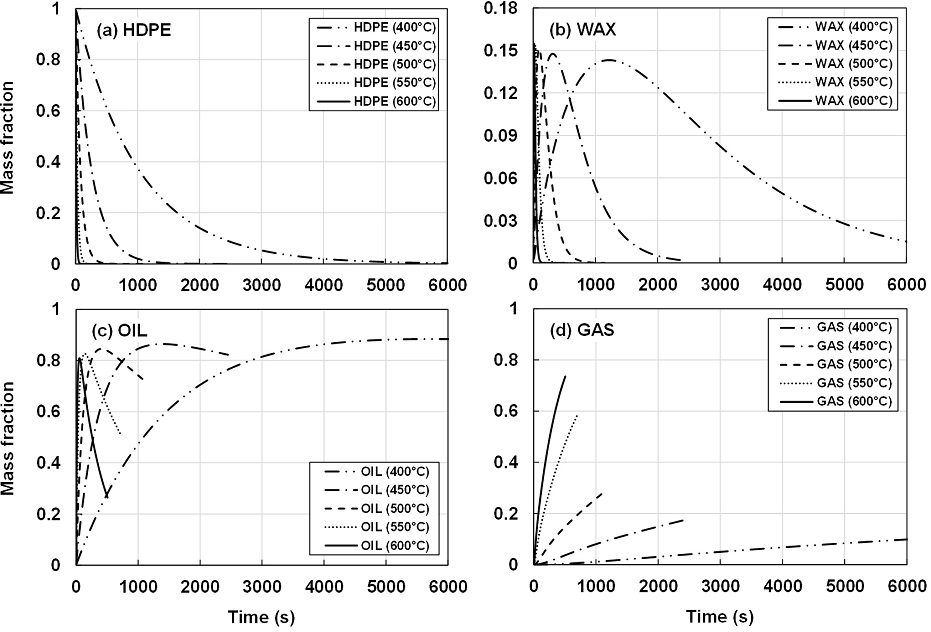
Mass fractions of (a) HDPE, (b) wax, (c) oil, and (d) gas for HDPE pyrolysis at various reaction temperatures
LDPE의 시간에 따른 열분해는 Fig. 5(a)에서와 같이 HDPE에 비하여 다소 느리게 발생하며, 이에 따라 Fig. 5(b), (c)에서와 같이 왁스 및 오일의 증가 및 감소 또한 느리게 일어난다. 왁스의 최대 분율은 HDPE보다 매우 크게 나타나는데, 400℃에서는 약 3배이고 600℃에서는 약 2.5배이다. 또한 온도에 따른 왁스의 최대 분율 변화를 살펴보면 HDPE에서와는 반대로 온도 증가에 따라 조금씩 감소하는 경향을 보인다. 온도에 따른 오일의 최대 분율은 HDPE에서와 같이 온도 증가에 따라 감소하는데, 각 온도에서 오일의 최대 분율은 HDPE에 비하여 낮다. 가스의 생성은 Fig. 5(d)에서와 같이 500℃ 이상의 온도에서는 Fig. 4(d)에 나타난 HDPE의 경우에 비하여 빨라지는 특성이 있는데, 600℃에서는 계산 시간 범위 내에서 가스의 질량 분율이 0.8 이상까지 증가하므로 이러한 온도는 오일보다는 가스 생산에 적합할 것으로 보인다.
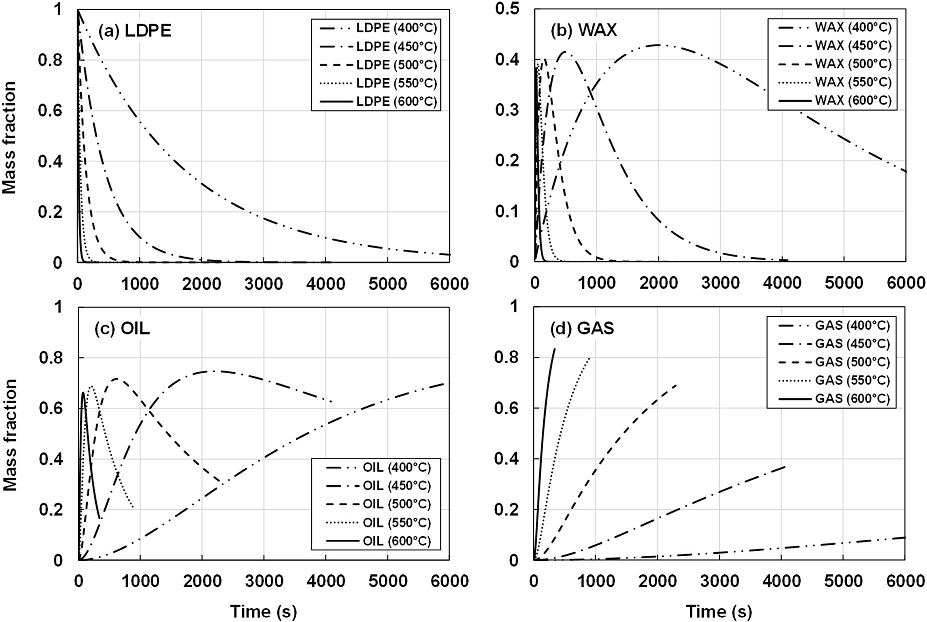
Mass fractions of (a) LDPE, (b) wax, (c) oil, and (d) gas for LDPE pyrolysis at various reaction temperatures
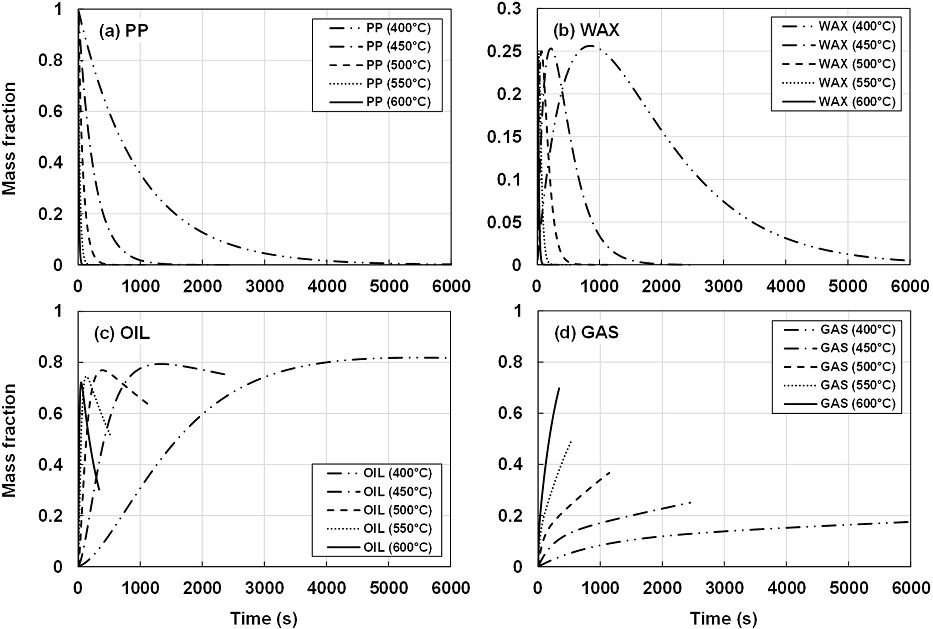
Fig. 6(a)는 다양한 온도에서 PP의 시간에 따른 질량 분율 변화를 나타낸다. PP의 열분해 속도는 Fig. 4(a)에 나타난 HDPE의 경우와 유사한 특성을 보인다. 그러나 Fig. 6(b)에 나타난 왁스의 증가 및 감소는 Fig. 4(b)에 나타난 HDPE의 경우와 비교하여 보았을 때 다소 빠르게 발생하며, 왁스의 최대값은 HDPE에서와는 반대로 온도에 따라 조금씩 감소한다. 또한 각 온도에서 왁스의 최대값은 HDPE보다는 높고 LDPE보다는 낮다. 오일의 증가 및 감소 속도는 Fig. 6(c)에 나타난 것과 같이 HDPE와 유사하며, 온도 변화에 따른 오일의 최대값은 HDPE, LDPE에서와 같이 온도 증가에 따라 감소한다. 가스의 생성은 Fig. 6(d)에서와 같이 온도 증가에 따라 빨라지는데, 각 온도에서의 증가 추이를 살펴보면 초반에 빠르게 발생하다가 그 증가 속도가 조금씩 느려짐을 알 수 있다.
3.3 온도별 열분해 시간 및 오일 분율 비교
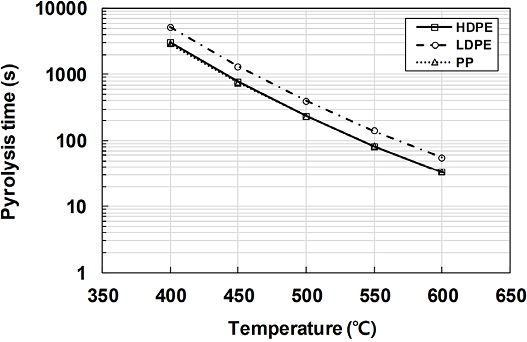
각 플라스틱 종류별로 다양한 온도에서의 열분해 속도를 구체적으로 비교해 보기 위하여, 각 온도에서 플라스틱의 질량 분율이 0.05 이하로 감소하는 시점을 열분해 시간(pyrolysis time)으로 정의하고 Fig. 7에 나타내었다.
Fig. 4-6에서와 같이 플라스틱의 열분해는 온도 증가에 따라 급격히 빨라지기 때문에 Fig. 7의 로그 눈금에서는 온도에 따라 거의 선형적으로 감소하는 모양이 된다. HDPE의 경우 400℃에서는 열분해에 3,000초 이상이 소요되지만 450℃에서는 열분해 시간이 770초로 빠르게 감소하고, 600℃에서는 33초로 짧아진다. HDPE와 PP의 열분해 시간은 거의 유사하고, LDPE의 열분해 시간은 모든 온도에서 HDPE, PP보다 약 1.7배 길기 때문에 전반적으로 LDPE의 열분해는 다른 플라스틱에 비하여 많은 시간이 소요됨을 알 수 있다.
기존의 선행 연구에서 수행된 열중량 분석 결과에 의하면, LDPE가 HDPE에 비하여 열분해 속도가 빠르고[30~33] PP는 PE에 비하여 열분해 속도가 빠른 것으로 나타난다.[28,32,33] 이론적으로도 LDPE의 경우 HDPE에 비하여 탄소 사슬의 분기가 많아 분자간 힘이 더 작은 것으로 알려져 있으므로,[25,29] LDPE의 열분해가 HDPE보다 빨리 일어나는 것이 타당하다. 또한 PP의 경우 1,2차 탄소에 비해 분해되기 쉬운 3차 탄소의 개수가 PE보다 많기 때문에 열분해 시간이 더 짧게 소요되는 것으로 알려져 있다.[25,28,29] 이러한 선행 연구 결과는 본 연구에서 도출된 열분해 시간과는 경향이 다르기 때문에, 그 원인에 관하여 추가적인 고찰을 수행하였다. 우선 열중량 분석의 경우 상온으로부터 시작하여 일정한 승온 속도를 가지고 온도가 상승하면서 열분해가 이루어지는 것에 비하여, 본 연구에서는 등온 조건에서 PFR 해석을 수행하였기 때문에 차이가 발생할 수 있다. 특히 HDPE, LDPE, PP 등의 플라스틱은 400℃ 이하의 온도부터 열분해가 시작되는데[29] 본 연구에서 사용된 반응속도 상수는 450℃-550℃의 온도범위에 최적화되어 있어 차이가 발생할 가능성도 존재한다. 따라서 더 낮은 온도에서 도출된 다른 선행 연구에서의 반응속도 상수를 이용하면서, 상온으로부터 온도를 상승시키는 조건에서의 추가적인 후속 연구가 필요할 것으로 생각된다.
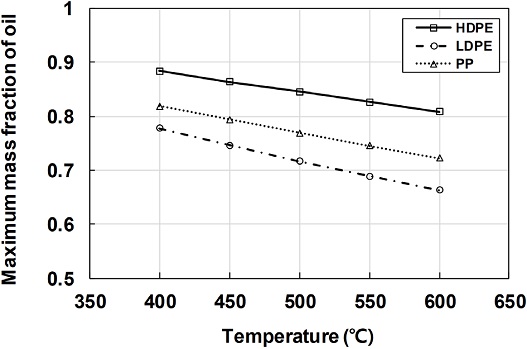
플라스틱 열분해의 주요 목적을 오일 생산으로 하였을 때를 가정하여 각 플라스틱의 온도에 따른 최대 오일 분율을 Fig. 8에 나타내었다. 최대 오일 분율은 모든 플라스틱 종류에 대하여 온도에 따라 거의 선형적으로 감소한다. HDPE의 최대 오일 분율은 400℃에서 약 0.88이었다가 600℃에서 0.81이 되고, LDPE의 최대 오일 분율은 400℃에서 0.78이고 600℃에서는 0.66으로 감소한다. PP의 최대 오일 분율은 HDPE와 LDPE의 사이에 존재한다. 본 연구에서 도출된 온도별 최대 오일 분율은 이상적인 상태에서 계산된 값이기 때문에 실제 열분해반응기에서 얻을 수 있는 오일의 수율은 계산값보다 작을 것으로 보이며, Fig. 4-6에서와 같이 오일의 분율은 최대값에 도달하였다가 시간이 경과하면서 감소하기 때문에 오일의 생산을 최대로 하기 위해서는 반응기 내 체류 시간을 적절히 조절할 필요가 있을 것으로 생각된다.
4. 결 론
다양한 플라스틱의 기본적인 열분해 특성을 비교해 보기 위하여, plug flow reactor(PFR) 모델을 이용한 해석을 수행하였다. 열분해 생성물을 왁스, 오일, 가스로 단순화한 집중 반응속도 모델(lumped kinetic model)을 적용하여 시간에 따른 HDPE, LDPE, PP의 열분해 과정을 모사하였다. 플라스틱의 열분해는 온도 증가에 따라 급격히 빨라지고, 왁스 및 오일은 시간이 경과하면서 증가하였다가 감소하며 가스는 지속적으로 증가하는 특성을 보인다. LDPE의 열분해에서는 왁스가 많이 생성되고, 열분해 시간은 HDPE와 PP에 비하여 많이 소요되는 특성이 있다. 열분해에서 얻을 수 있는 최대 오일 분율은 일정한 온도에서 HDPE, PP, LDPE 순으로 나타나고, 온도 증가에 따라 감소한다.
본 연구는 1D 형상으로 단순화된 모델을 이용하여 수행되었으므로, 실제 열분해반응기에서 발생하는 플라스틱 및 생성물의 이송 및 열전달 특성 등을 포함하지 않는 한계가 있다. 또한 등온 조건에서 해석이 이루어졌고 반응속도 상수가 450℃-550℃의 제한된 온도 범위에서 최적화되어 있어 플라스틱별 열분해 시간 비교 결과가 기존의 선행 연구로부터 알려진 실험 결과와 차이가 발생하였다. 따라서 다양한 집중 반응속도 모델(lumped kinetic model)을 이용한 비등온 조건에서의 후속 연구가 필요할 것으로 생각되며, 이러한 집중 반응속도 모델은 추후 열분해반응기에 대한 CFD 해석에도 적용 가능할 것으로 기대된다.
Acknowledgments
본 연구는 2022년 중소벤처기업부의 “연속 투입과 배출이 가능하고 폐수와 미세먼지 발생이 없는 폐플라스틱 열분해 유화 공정 개발”(과제번호: S3264002)의 일환으로 수행되었으며 이에 감사드립니다.
References
-
Lee, S.H., 2019, “Current status of plastic recycling in Korea”, J. of Korean Inst. of Resources Recycling, 28(6), 3-8.
[https://doi.org/10.7844/kirr.2019.28.6.3]

-
Cho, Y.J., and Cho, B.G., 2020, “Status and future prospects for plastics recycling”, J. of Korean Inst. of Resources Recycling, 29(4), 31-44.
[https://doi.org/10.7844/kirr.2020.29.4.31]

-
Lee, K.J., 2015, “The reaction kinetic study of SRF and industrial waste using TGA (Thermo Gravimetric Analysis)”, New. Renew. Energy, 11(1), 20-26.
[https://doi.org/10.7849/ksnre.2015.03.1.020]

-
Chae, J.S., Yang, S.J., Kim, S.W., Lee, J.H., and Ohm, T.I., 2020, “A study on the combustion characteristics of food waste using the experimental apparatus for combustibility”, New. Renew. Energy, 16(2), 47-53.
[https://doi.org/10.7849/ksnre.2020.2061]

-
Yoon, H.C., Cho, S.H., Lee, D.J., Moon, G.Y., and Cho, S.H., 2016, “A study on the optimal operating condition of a Dual Fluidized-Bed (DFB) with biomass and SRF”, New. Renew. Energy, 12(4), 77-87.
[https://doi.org/10.7849/ksnre.2016.12.12.4.077]

-
Dogu, O., Pelucchi, M., Van de Vijver, R., Van Steenberge, P.H.M., D’hooge, D.R., Cuoci, A, Mehl, M., Frassoldati, A., Faravelli, T., and Van Geem, K.M., 2021, “The chemistry of chemical recycling of solid plastic waste via pyrolysis and gasification: State-of-the-art, challenges, and future directions”, Prog. Energy Combus. Scie., 84, 100901.
[https://doi.org/10.1016/j.pecs.2020.100901]

-
Ranzi, E., Dente, M., Faravelli, T., Bozzano, G., Fabini, S., Nava, R., Cozzani, V., and Tognotti, L., 1997, “Kinetic modeling of polyethylene and polypropylene thermal degradation”, J. Anal. Appl. Pyrolysis., 40-41, 305-319.
[https://doi.org/10.1016/S0165-2370(97)00032-6]

-
Westerhout, R.W.J., Waanders, J., Kuipers, J.A.M., and van Swaaij, W.P.M., 1997, “Kinetics of the low-temperature pyrolysis of polyethene, polypropene, and polystyrene modeling, experimental determination, and comparison with literature models and data”, Ind. Eng. Chem. Res., 36(6), 1955-1964.
[https://doi.org/10.1021/ie960501m]

-
Bockhorn, H., Hornung, A., Hornung, U., and Schawaller, D., 1999, “Kinetic study on the thermal degradation of polypropylene and polyethylene”, J. Anal. Appl. Pyrolysis., 48(2), 93-109.
[https://doi.org/10.1016/S0165-2370(98)00131-4]

-
Kruse, T.M., Wong, H.W., and Broadbelt, L.J., 2003, “Mechanistic modeling of polymer pyrolysis: Polypropylene”, Macromolecules, 36(25), 9594-9607.
[https://doi.org/10.1021/ma030322y]

-
Elordi, G., Lopez, G., Olazar, M., Aguado, R., and Bilbao, J., 2007, “Product distribution modelling in the thermal pyrolysis of high density polyethylene”, J. Hazard. Mater., 144(3), 708-714.
[https://doi.org/10.1016/j.jhazmat.2007.01.101]

-
Costa, P.A., Pinto, F.J., Ramos, A.M., Gulyurtlu, I.K., Cabrita, I.A., and Bernardo, M.S., 2007, “Kinetic evaluation of the pyrolysis of polyethylene waste”, Energy Fuels, 21(5), 2489-2498.
[https://doi.org/10.1021/ef070115p]

-
Németh, A., Blazsó, M., Baranyai, P., and Vidóczy, T., 2008, “Thermal degradation of polyethylene modeled on tetracontane”, J. Anal. Appl. Pyrolysis, 81(2), 237-242.
[https://doi.org/10.1016/j.jaap.2007.11.012]

-
Levine, S.E., and Broadbelt, L.J., 2009, “Detailed mechanistic modeling of high-density polyethylene pyrolysis: Low molecular weight product evolution”, Polymer Degradation and Stability, 94(5), 810-822.
[https://doi.org/10.1016/j.polymdegradstab.2009.01.031]

-
Costa, P., Pinto, F., Ramos, A.M., Gulyurtlu, I., Cabrita, I., and Bernardo, M.S., 2010, “Study of the pyrolysis kinetics of a mixture of polyethylene, polypropylene, and polystyrene”, Energy Fuels, 24(12), 6239-6247.
[https://doi.org/10.1021/ef101010n]

-
Al-Salem, S.M., and Lettieri, P., 2010, “Kinetic study of high density polyethylene (HDPE) pyrolysis”, Chemical Engineering Research and Design, 88(12), 1599-1606.
[https://doi.org/10.1016/j.cherd.2010.03.012]

-
Ding, F., Xiong, L., Luo, C., Zhang, H., and Chen, X., 2012, “Kinetic study of low-temperature conversion of plastic mixtures to value added products”, J. Anal. Appl. Pyrolysis., 94, 83-90.
[https://doi.org/10.1016/j.jaap.2011.11.013]

-
Gascoin, N., Navarro-Rodriguez, A., Gillard, P., and Mangeot, A., 2012, “Kinetic modelling of high density polyethylene pyrolysis: Part 1. Comparison of existing models”, Polymer Degradation and Stability, 97(8), 1466-1474.
[https://doi.org/10.1016/j.polymdegradstab.2012.05.008]

-
Gascoin, N., Navarro-Rodriguez, A., Fau, G., and Gillard, P., 2012, “Kinetic modelling of High Density PolyEthylene pyrolysis: Part 2. Reduction of existing detailed mechanism”, Polymer Degradation and Stability, 97(7), 1142-1150.
[https://doi.org/10.1016/j.polymdegradstab.2012.04.002]

-
Csukás, B., Varga, M., Miskolczi, N., Balogh, S., Angyal, A., and Bartha, L., 2013, “Simplified dynamic simulation model of plastic waste pyrolysis in laboratory and pilot scale tubular reactor”, Fuel Process. Technol., 106, 186-200.
[https://doi.org/10.1016/j.fuproc.2012.07.024]

-
Zhang, H.R., Ding, F., Luo, C.R., and Chen, X.D., 2015, “Kinetics of the low temperature conversion of polypropylene to polypropylene wax”, Energy Sources, Part A: Recovery, Utilization, and Environmental Effects, 37(15), 1612-1619.
[https://doi.org/10.1080/15567036.2011.631974]

-
Eidesen, H., Khawaja, H., and Jackson, S., 2018, “Simulation of the HDPE pyrolysis process”, Int. J. Multiphysics, 12(1), 79-88.
[https://doi.org/10.21152/1750-9548.12.1.79]

-
Lechleitner, A.E., Schubert, T., Hofer, W., and Lehner, M., 2021, “Lumped kinetic modeling of polypropylene and polyethylene co-pyrolysis in tubular reactors”, Processes, 9(1), 34.
[https://doi.org/10.3390/pr9010034]

-
Harmon, R.E., SriBala, G., Broadbelt, L.J., and Burnham, A.K., 2021, “Insight into polyethylene and polypropylene pyrolysis: Global and mechanistic models”, Energy Fuels, 35(8), 6765-6775.
[https://doi.org/10.1021/acs.energyfuels.1c00342]

-
Kulas, D.G., Zolghadr, A., and Shonnard, D., 2021, “Micropyrolysis of polyethylene and polypropylene prior to bioconversion: The effect of reactor temperature and vapor residence time on product distribution”, ACS Sustainable Chem. Eng., 9(43), 14443-14450.
[https://doi.org/10.1021/acssuschemeng.1c04705]

-
Jiang, G., Fenwick, R., Seville, J., Mahood, H.B., Thorpe, R.B., Bhattacharya, S., Sanchez Monsalve, D.A., and Leeke, G.A., 2022, “Lumped kinetic modelling of polyolefin pyrolysis: A non-isothermal method to estimate rate constants”, J. Anal. Appl. Pyrolysis., 164, 105530.
[https://doi.org/10.1016/j.jaap.2022.105530]

- Goodwin, D.G., Moffat, H.K., Schoegl, I., Speth, R.L., and Weber, B.W.. 2022, “Cantera: An object-oriented software toolkit for chemical kinetics, thermodynamics, and transport processes”, Version 2.6.0., Accessed 22 November 2022, https://www.cantera.org, .
-
Jung, S.H., Cho, M.H., Kang, B.S., and Kim, J.S., 2010, “Pyrolysis of a fraction of waste polypropylene and polyethylene for the recovery of BTX aromatics using a fluidized bed reactor”, Fuel Process. Technol., 91(3), 277-284.
[https://doi.org/10.1016/j.fuproc.2009.10.009]

-
Sharuddin, S.D.A., Abnisa, F., Daud, W.M.A.W., and Aroua, M.K., 2016, “A review on pyrolysis of plastic wastes”, Energy Convers. Manag., 115, 308-326 .
[https://doi.org/10.1016/j.enconman.2016.02.037]

-
Park, J.W., Oh, S.C., Lee, H.P., Kim, H.T., and Yoo, K.O., 2000, “Kinetic analysis of thermal decomposition of polymer using a dynamic model”, Korean J. Chem. Eng., 17(5), 489-496.
[https://doi.org/10.1007/BF02707154]

-
Kayacan, İ., and Doğan, Ö.M., 2008, “Pyrolysis of low and high density polyethylene. Part I: Non-isothermal pyrolysis kinetics”, Energy Sources, Part A: Recovery, Utilization, and Environmental Effects, 30(5), 385-391.
[https://doi.org/10.1080/15567030701457079]

-
Aboulkas, A., El harfi, K., and El Bouadili, A., 2010, “Thermal degradation behaviors of polyethylene and polypropylene. Part I: Pyrolysis kinetics and mechanisms”, Energy Conversion and Management, 51(7), 1363-1369.
[https://doi.org/10.1016/j.enconman.2009.12.017]

-
Saad, J.Md., Williams, P.T., Zhang, Y.S., Yao, D., Yang, H., and Zhou, H., 2021, “Comparison of waste plastics pyrolysis under nitrogen and carbon dioxide atmospheres: A thermogravimetric and kinetic study”, J. Anal. Appl. Pyrolysis., 156, 105135.
[https://doi.org/10.1016/j.jaap.2021.105135]